Anomeeri
Anomeerit ovat IUPAC:n määritelmän mukaan sokereiden syklisten muotojen diastereomeereja, joilla ainoastaan yhden hiilen konfiguraatio on erilainen. Aldooseilla ero on C-1-hiilessä ja ketooseilla C-2-hiilessä.[1] Tämä tarkoittaa hemiasetaalin tai hemiketaalin hydroksyyliryhmän asentoa renkaaseen nähden.[2]
Nimeäminen[muokkaa | muokkaa wikitekstiä]
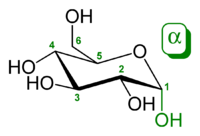
Sokerit voivat olla liuoksissa kahtena rengasmaisena muotona, furanoosina ja pyranoosina, jotka eroavat toisistaan renkaan hiiliatomien määrän perusteella. Kun avoketjuinen sokerimolekyyli muuntuu rengasrakenteiseksi, molekyyliin muodostuu uusi kiraalinen hiiliatomi, jota kutsutaan anomeeriseksi hiileksi. Jos tähän hiileen liittynyt niin kutsuttu anomeerinen hydroksyyliryhmä osoittaa rengasrakenteen tasoon nähden alaspäin, sitä nimitetään d-tyypin sokerimolekyylin tapauksessa α-anomeeriksi, l-tyypin sokerilla kyseessä on β-anomeeri. Jos hydroksyyliryhmän suunta on ylöspäin, kyseessä on d-tyypin sokerimolekyylin tapauksessa β-anomeeri, l-tyypin sokerilla kyseessä on α-anomeeri. Jos molekyylin stereoisomerian kuvaamiseen käytetään d- ja l-kirjaimia, tulee anomeerimuodon osoittava kreikkalainen kirjain ennen niitä, esimerkiksi α-d-glukopyranoosi.[2][3] d- ja l-kirjaimet kirjoitetaan IUPAC:n ohjeiden mukaisesti kapiteelilla (engl. small caps).[4]
 |

|
|
|
Ominaisuudet[muokkaa | muokkaa wikitekstiä]
Vesiliuoksissa sokerimolekyylien ja niiden johdannaisten α- ja β-anomeerit ovat keskenään tasapainossa. Anomeerien suhteeseen vaikuttaa anomeerinen efekti. Stereoelektroniikasta ja liuoksen olosuhteista johtuva anomeerinen efekti aiheuttaa sen, että elektronegatiivisen atomin sisältävä ryhmä on niin sanotussa aksiaalisessa asemassa ja α-anomeerina. Glukoosi on poikkeus ja esiintyy vesiliuoksissa pääasiassa β-anomeerina.[5]
Anomeerit vaikuttavat sokeripolymeerien ominaisuuksiin, esimerkiksi niiden sulavuuteen ihmisen elimistössä. Tärkkelys, koostuu glukoosin α-anomeerista ja selluloosa β-anomeerista. Ihminen voi hyödyntää ravintonaan tärkkelystä, mutta ei selluloosaa.[6]
Sokeriliuosten kyky kiertää valon polarisaatiota muuttuu ajan kuluessa ja saavuttaa lopulta vakioarvon. Tämä johtuu anomeerien muuntumisesta toisikseen, ja tätä prosessia kutsutaan mutarotaatioksi.[2]
Anomerisoituminen[muokkaa | muokkaa wikitekstiä]
Mutarotaation lisäksi anomeerit voivat muuttua toisikseen myös anomerisoitumisen kautta. Anomerisoituminen eroaa mutarotaatiosta hieman mekanismiltaan ja voi tapahtua myös aproottisissa liuoksissa. Anomerisoitumisessa happokatalyytti hajottaa renkaan C-1-hiilen ja happiatomin välisen sidoksen, jolloin muodostuu avoketjuinen välimuoto. C-1- ja C-2-hiilen välinen sidos pääsee kiertymään ja renkaan jälleen sulkeuduttua on molekyyli toisena anomeerinaan.[7]

Anomeerikonfiguraation määritys[muokkaa | muokkaa wikitekstiä]
Syklisen molekyylin konformaation määritys on hankalaa ja edellyttää, että molemmat muodot on onnistuttu eristämään. Anomeerien vetyatomeilla on erilaiset dihedraalikulmat, jotka tulevat esiin H-NMR-spektroskopialla eri suuruisina kytkentävakioina. α-anomeerien dihedraalikulmat ovat tyypillisesti β-anomeerien kulmia pienemmät, ja tällöin niiden kytkentävakio on myös pienempi, mikä näkyy NMR-spektrometrin antamissa tuloksissa piikkien muodossa.[8]
Lähteet[muokkaa | muokkaa wikitekstiä]
- ↑ Anomers IUPAC Gold Book. International Union of Pure and Applied Chemistry. Viitattu 23.6.2010. (englanniksi)
- ↑ a b c Raimo Alén: Kokoelma orgaanisia yhdisteitä, s. 938. Consalen Consulting, 2009. ISBN 978-952-92-5627-3.
- ↑ Nomenclature of Carbohydrates (Recommendations 1996) Queen Mary, University of London. Viitattu 23.6.2010. (englanniksi)
- ↑ 2-Carb-4.1. Use of D and L Nomenclature of Carbohydrates (Recommendations 1996). 1996. Queen Mary, University of London. Viitattu 11.5.2012. (englanniksi)
- ↑ Andrew Miller,Julian Tanner: Essentials of chemical biology, s. 29. John Wiley and Sons, 2008. ISBN 978-0-470-84530-1. Kirja Googlen teoshaussa (viitattu 23.06.2010). (englanniksi)
- ↑ Vickie Vaclavik,Vickie A. Vaclavik,Elizabeth W. Christian: Essentials of food science, s. 39. Springer, 2008. ISBN 978-0-387-69939-4. Kirja Googlen teoshaussa (viitattu 23.06.2010). (englanniksi)
- ↑ Momčilo Miljković: Carbohydrates: Synthesis, Mechanisms, and Stereoelectronic Effects, s. 105. Springer, 2009. ISBN 978-0-387-92264-5. Kirja Googlen teoshaussa (viitattu 23.06.2010). (englanniksi)
- ↑ Joseph M. Hornback: Organic Chemistry, s. 1095. Cengage Learning, 2005. ISBN 978-0534389512. Kirja Googlen teoshaussa (viitattu 23.06.2010). (englanniksi)
| Pääjoukko | |
|---|---|
| Geometria |
pentoosit • heksoosit • heptoosi • sykloheksaanikonformaatio • anomeeri • mutarotaatio |
| Suuri / pieni |
glyseraldehydi • dihydroksiasetoni • erytroosi • treoosi • erytruloosi • sedoheptuloosi |
| Pentoosit |
riboosi • arabinoosi • ksyloosi • lyksoosi • ribuloosi • ksyluloosi |
| Heksoosit |
glukoosi • galaktoosi • mannoosi • guloosi • idoosi • taloosi • alloosi • altroosi • fruktoosi • sorboosi • tagatoosi • psikoosi • fukoosi • ramnoosi |
| Disakkaridit |
sakkaroosi • laktoosi • trehaloosi • maltoosi • sellobioosi |
| Polysakkaridit |
glykogeeni • tärkkelys • selluloosa • kitiini • amyloosi • amylopektiini • stakyoosi • inuliini • dekstriini • pullulaani |
| Glykosaminoglykaanit |
hepariini • kondroitiinisulfaatti • hyaluronaani • heparaanisulfaatti • dermataanisulfaatti • kerataanisulfaatti |
| Aminoglykosidit |
kanamysiini • streptomysiini • tobramysiini • neomysiini • paromomysiini • apramysiini • gentamisiini • netilmysiini • amikasiini |