Hemiasetaalit


Hemiasetaali on yhdiste, joka sisältää samaan hiiliatomiin kiinnittyneenä sekä hydroksyyli- että eetteriryhmän. Hemiasetaalia voidaan pitää aldehydin ja alkoholin additiotuotteena. Samalla tavalla ketoneista muodostuu hemiketaaleja, joita IUPAC:in nimistössä pidetään hemiasetaalien alaluokkana. Syklisiä hemiasetaaleja nimitetään laktoleiksi.[1][2][3][4][5]
Valmistus ja ominaisuudet[muokkaa | muokkaa wikitekstiä]
Hemiasetaaleja voidaan valmistaa alkoholien ja aldehydien välisellä reaktiolla, joka on tyypiltään nukleofiilinen substituutioreaktio karbonyyliryhmään. Tässä reaktiossa käytetään tyypillisesti joko happo- tai emäskatalyyttiä. Happokatalyytti protonoi karbonyyliryhmän happiatomin, jolloin hiiliatomista tulee vieläkin elektrofiilisempi. Nukleofiilinen alkoholimolekyyli hyökkää karbonyyliryhmään, jolloin muodostuu tetraedrimäinen välituote, josta muodostuu hemiasetaali deprotonoitumisen seurauksena. Emäskatalyytti tekee alkoholista alkoksidi-ionin, joka on nukleofiilisempi kuin alkoholimolekyyli. Alkoksidi-ioni hyökkää karbonyylihiileen ja muodostuneen välituotteen protonointi johtaa hemiasetaaliin. Sekä happo- että emäskatalyytit katalysoivat myös hemiasetaalin hydrolyysiä.[5]

Myös ketonit reagoivat happo- tai emäskatalysoituna hemiasetaaleja, joita kutsutaan hemiketaaleiksi. Nämä reaktiot ovat kuitenkin usein hitaampia kuin vastaavat aldehydien reaktiot.[5]

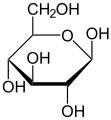
Hemiasetaali muodostuu välituotteena alkoholien ja aldehydien tai ketonien välisissä happokatalysoidussa reaktiossa, joissa muodostuu asetaaleja tai ketaaleja. Muodostuminen edellyttää usein ylimäärää alkoholia. Hemiasetaalit ovat useimmiten melko epästabiileja, eikä niitä saada eristetyksi liuoksista. Elektroneja puoleensa vetävät substituentit, kuten halogeenit kuitenkin lisäävät stabiiliutta. Sykliset hemiasetaalit eli laktolit sen sijaan ovat hyvinkin stabiileja ja luonnossa sokerimolekyylit esiintyvät liuoksissa hemiasetaalimuodoissaan furanooseina ja pyranooseina.[4][5]
-
Glukopyranoosi
-
Fruktofuranoosi
Lähteet[muokkaa | muokkaa wikitekstiä]
- ↑ Hemiacetal IUPAC GoldBook. IUPAC. Viitattu 4.5.2011. (englanniksi)
- ↑ Hemiketal IUPAC GoldBook. IUPAC. Viitattu 4.5.2011. (englanniksi)
- ↑ Lactol IUPAC GoldBook. IUPAC. Viitattu 4.5.2011. (englanniksi)
- ↑ a b Raimo Alén: Kokoelma orgaanisia yhdisteitä, s. 248, 938. Consalen Consulting, 2009. ISBN 978-952-92-5627-3.
- ↑ a b c d Jonathan Clayden, Nick Greeves, Stuart Warren, Peter Wothers: Organic Chemistry, s. 145–147, 340–343. Oxford University Press, 2008. ISBN 978-0-19-850346-0. (englanniksi)
Aiheesta muualla[muokkaa | muokkaa wikitekstiä]
 Kuvia tai muita tiedostoja aiheesta Hemiasetaalit Wikimedia Commonsissa
Kuvia tai muita tiedostoja aiheesta Hemiasetaalit Wikimedia Commonsissa