Liuos


Liuos on seos jossa kaksi tai useampia aineita on sekoittunut toisiinsa muodostaen yhtenäisen faasin. Liuos on kyseessä silloin, kun ainehiukkaset eivät ole havaittavissa edes mikroskoopilla, eivätkä saostu liuoksen seistessä suljetussa astiassa. Yleensä liuoksesta puhuttaessa tarkoitetaan nestemäisiä seoksia, jotka syntyvät jonkin aineen liuetessa nestemäiseen liuottimeen[1], mutta laajemmassa mielessä liuos voi olla myös kiinteä aine tai kaasu[2].
Aineen liukoisuus johonkin liuottimeen voi olla rajallinen; tällöin muodostuu kylläinen liuos ja ylimääräinen aine erottuu omaksi faasikseen. Jotkin aineet kuitenkin liukenevat toisiinsa missä suhteessa tahansa. Tällöin sanotaan tavallisesti liuoksen runsainta komponenttia liuottimeksi ja muita aineita liuenneiksi aineiksi.[2]
Tyypillisiä piirteitä[muokkaa | muokkaa wikitekstiä]
Liuos on homogeeninen seos. Liuenneen aineen hiukkasia ei siinä voi nähdä paljain silmin. Valo ei siroa liuoksessa olevista liuenneen aineen hiukkasista. Liuennutta ainetta ei voi eristää liuoksesta suodattamalla tai mekaanisesti.
Liuostyyppejä ja esimerkkejä[muokkaa | muokkaa wikitekstiä]
Liuoksen homogeenisuus merkitsee sitä, että sen komponentit muodostavat yhden faasin. Sen olomuoto on sama kuin liuottimen. Kuitenkin aineen ominaisuudet kuten sulamis- ja kiehumispiste tyypillisesti muuttuvat, kun siihen sekoittuu muita aineita.
Kaasumaiset liuokset[muokkaa | muokkaa wikitekstiä]
Jos liuotin on kaasu, siihen voivat yleensä liueta vain toiset kaasut. Esimerkkinä kaasumaisesta liuoksesta voidaan mainita ilma, jossa happi ja muut kaasut ovat liuenneet typpeen. Koska molekyylien välisillä vuorovaikutuksilla ei kaasuissa ole sanottavaa merkitystä, pieninä pitoisuuksina esiintyvät kaasut muodostavat varsin triviaaleja liuoksia. Usein niitä ei edes nimitetä liuoksiksi vaan kaasuseoksiksi.
Nestemäiset liuokset[muokkaa | muokkaa wikitekstiä]
Nestemäiseen liuottimeen voivat liueta sekä kiinteät aineet, nesteet että kaasut.
Periaatteessa kaikenlaiset nesteet voivat toimia liuottimina: nestemäiset jalokaasut, sulat metallit, sulat suolat, sulaneet kovalenttiset aineet ja molekyyleistä koostuneet nesteet. Käytännössä useimmat kemiassa ja biokemiassa merkittävät liuottimet kuitenkin ovat molekyyleistä koostuvia nesteitä. Ne voidaan jakaa poolisiin ja poolittomiin sen mukaan, onko niiden molekyyleillä pysyvä sähköinen dipolimomentti. Toisaalta ne voidaan jaotella sen mukaan, voivatko niiden molekyylit muodostaa vetysidoksia; tämän mukaisesti puhutaan proottisista ja aproottisista liuottimista. Yleisin liuotin, vesi, on poolinen, ja siinä on vetysidoksia.
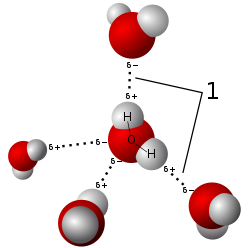
Suolat liukenevat poolisiin liuottimiin muodostaen positiivisia ja negatiivisia ioneja, joita liuottimen molekyylin negatiivinen ja positiivinen pää vetävät puoleensa. Tällaiset liuokset ovat elektrolyyttejä.
Kun liukeneva aine ei ole ioniyhdiste, yleinen sääntö on: samanlainen liuottaa samanlaista.[2]
Pooliset aineet liukenevat poolisiin liuottimiin. Esimerkiksi sokeri ja etanoli ovat poolisia aineita ja liukenevat hyvin veteen. Sitä vastoin poolittomat aineet liukenevat paremmin poolittomiin liuottimiin. Esimerkiksi maaöljyssä olevat hiilivedyt liukenevat hyvin toisiinsa ja liuottavat myös kiinteitä hiilivetyjä, jotka eivät liukene veteen, kuten eivät myöskään maaöljyssä olevat nestemäiset hiilivedyt. Tämän vuoksi öljyonnettomuuksissa öljy ei liukene meriveteen vaan jää kellumaan sen pinnalle.
Nesteeseen liuenneet kaasut[muokkaa | muokkaa wikitekstiä]
Kaasuista esimerkiksi happea esiintyy liuenneena luonnonvesissä. Myös hiilidioksidi liukenee veteen, mutta ilmiö on tällöin hieman monimutkaisempi, koska tapahtuu kemiallinen reaktio, jossa syntyy pieniä määriä hiilihappoa[3] ja sen happoluonteen vuoksi edelleen oksonium- ja vetykarbonaatti-ioneja. Hiilihappoisessa vedessä ja esimerkiksi virvoitusjuomissa olevat näkyvät kuplat eivät kuitenkaan ole liuennutta kaasua, vaan niissä oleva hiilidioksidi on jo erottunut liuoksesta omaksi kaasumaiseksi faasikseen. Liuennut kaasu itse ei ole näkyvää, koska se on liuennut molekyylitasolla.
Nesteeseen liuenneet nesteet[muokkaa | muokkaa wikitekstiä]
Maaöljy ja siitä valmistetut tuotteet kuten bensiini sekä kevyt ja raskas polttoöljy koostuvat pääasiassa toisiinsa liuenneista nestemäisistä hiilivedyistä.
Etyylialkoholi eli etanoli ja vesi liukenevat toisiinsa missä suhteessa tahansa. Alkoholijuomat ovat pääasiassa etanolin vesiliuoksia, joskin ne tavallisesti sisältävät muitakin aineita.
Nesteeseen liuenneet kiinteät aineet[muokkaa | muokkaa wikitekstiä]
Sokeri liukenee veteen molekyyleinä.
Natriumkloridi eli ruokasuola liukenee veteen ioneina kuten muutkin suolat, mikäli ne ovat vesiliukoisia. Tällaisten aineiden liuokset ovat elektrolyyttejä. Liuenneita suoloja, pääasiassa natriumkloridia, esiintyy luonnossa runsaasti merivedessä.
Myös vesijohtovesi on liuos, koska se sisältää ioneja (mm. kalsium- ja magnesiumioneja, vetykarbonaatti-ioneja, kloridi- ja sulfaatti-ioneja) sekä liuennutta kaasua (mm. happea).
Esimerkiksi kehon nesteet ovat liuoksia, joissa on monia liuenneita aineita. Monet niistä ovat elektrolyyttejä, sillä liuenneet aineet kuten kalium ovat ioneina. Lisäksi ne voivat sisältää molekyyleinä liuenneita aineita kuten sokeria ja ureaa. Liuenneella hapella ja hiilidioksidilla on myös suuri merkitys veren kemiassa, sillä huomattava muutos niiden pitoisuuksissa voi olla vakavan sairauden merkki.
Ei-homogeeniset aineet[muokkaa | muokkaa wikitekstiä]
On olemassa myös nestemäisiä seoksia, jotka eivät ole homogeenisia, esimerkiksi kolloidit, suspensiot ja emulsiot. Sellaisia ei pidetä liuoksina. Myöskään esimerkiksi kahvi ei ole liuos, vaikka se vaikuttaa kirkkaalta. Kahvin seistessä astiaan jää ruskea saostuma kun liuoksessa olevat hiukkaset eroavat nesteestä. Suodatinkahvi on kolloidinen seos. Myöskään maito ei ole liuos vaan kolloidinen seos, sillä se sisältää valkuaisaineita ja rasvaa pieninä pallosina. Pallosia ei voi nähdä, mutta ne aiheuttavat valon hajoamista (punerrus) valonsäteen kulkiessa maitokerroksen läpi.
Kiinteät liuokset[muokkaa | muokkaa wikitekstiä]
Jos liotin on kiinteä aine, se saattaa liuottaa sekä kaasuja, nesteitä että toisia kiinteitä aineita.
Kaasuista vety liukenee varsin hyvin moniin metalleihin, etenkin palladiumiin. Ilmiö on saanut osakseen käytännön mielenkiintoa varsinkin, koska sitä voidaan käyttää vedyn varastointiin.
Nesteistä esimerkiksi elohopea liukenee kultaan muodostaen amalgaamin. Nestemäinen heksaani liukenee parafiinivahaan.
Kahden tai useamman kiinteän aineen keskenään muodostamista liuoksista esimerkkeinä ovat useat metalliseokset, esimerkiksi pronssi. Teräksessä sen sijaan hiili on liuenneena rautaan.
Liuenneen aineen pitoisuus[muokkaa | muokkaa wikitekstiä]
Liuenneen aineen pitoisuus liuoksessa voidaan ilmoittaa esimerkiksi massaprosenttina, tilavuusprosenttina tai konsentraationa.
Esimerkkinä liuoksesta voidaan antaa tilanne, jossa 5,0 g ruokosokeria (C12H22O11) liuotetaan 100 ml:aan vettä, jolloin saadaan kirkas sokeriliuos.
Massaprosentti: 5 g / (5 + 100 g) = 4,7 %
Sokerin ainemäärä: n = m/M = 5 g / 342 g/mol
Molaarinen konsentraatio: c = n/V = 0,15 mol/l
Kylläinen liuos[muokkaa | muokkaa wikitekstiä]
Liuos on kylläinen, kun siihen ei enää liukene enempää ainetta, esimerkiksi sokeria. Kuitenkin vaikka liuos on tullut kylläiseksi sokerista, on mahdollista vielä liuottaa esimerkiksi suolaa. Useimpien aineiden liukoisuus riippuu liuottimen lämpötilasta siten, että kuumaan liuottimeen liukenee enemmän ainetta kuin kylmään.
Lähteet[muokkaa | muokkaa wikitekstiä]
- ↑ Otavan iso Fokus, 4. osa (Kr-Mn), s. 2336, art. Liuos. Otava, 1973. ISBN 951-1-00388-7.
- ↑ a b c Matti Tiilikainen & Ilkka Virtamo: Kemia 1, s. 55-60. WSOY, 1968.
- ↑ Otavan iso Fokus, 2. osa (Em-Io), s. 1072, art. Hiilidioksidi. Otava, 1973. ISBN 951-1-00272-4.
Aiheesta muualla[muokkaa | muokkaa wikitekstiä]
 Kuvia tai muita tiedostoja aiheesta Liuos Wikimedia Commonsissa
Kuvia tai muita tiedostoja aiheesta Liuos Wikimedia Commonsissa