Histidiini
| Histidiini | |
|---|---|
 |
|
| Koodit | His, H |
| Molekyylimassa | 155,16 |
| Sivuketjun tyyppi | emäs |
| Karboksyyliryhmän happovakio | 1,80 |
| Aminoryhmän happovakio | 9,33 |
| Sivuketjun happovakio | 6,04 |
| Isoelektrinen piste | 7,64 |
| Yleisyys proteiineissa | 2,3 % |
| Kodonit | CAU, CAC |
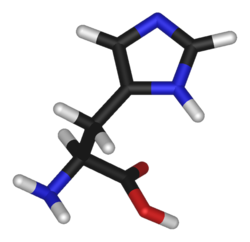
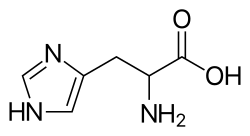
Histidiini (C6H9N3O2) on yksi elimistön solujen proteiinisynteesissä käytetyistä 20 perusaminohaposta. Se on lapsille ja myös aikuisille välttämätön aminohappo.
Histidiinin sivuketjun imidatsoli-renkaan happoparin happovakio on 6,04 ja histidiinin isoelektrinen piste on 7,64[1], minkä takia lieväkin happamuus muuttaa histidiinin varauksen neutraalista positiiviseksi. Tämän takia se on monien metalloproteiinien ligandi ja se sijaitsee useiden entsyymien katalyyttisessä keskuksessa. Histidiinilla on kaksi enantiomeeria eli peilikuvaisomeeria, jotka ovat L-histidiini ja D-histidiini. L-histidiinin CAS-numero on 71-00-1 ja D-histidiinin CAS-numero on 351-50-8.
Histidiini on histamiinin ja karnosiinin esiaste.
Aromaattisuus
[muokkaa | muokkaa wikitekstiä]Jotta yhdiste olisi aromaattinen, on siinä oltava tasomainen rengas, jonka atomeilla on yhteensä p-orbitaaleillaan pariton määrä elektronipareja, jotta delokalisaatio tapahtuisi koko renkaan alueella. Jokaisen atomin on oltava sp2- tai sp-hybridisoitunut ainakin jossain resonanssikontribuuttorissa.
Histidiinin sivuketju on aromaattinen, vaikkei sisälläkään fenyyliryhmää, sillä sen sivuketjun heterosyklisen renkaan toisen typen vapaa elektronipari on p-orbitaalilla (toisen taas sp2-orbitaalilla) – täten p-orbitaaleilla sijaitsevia elektronipareja on renkaassa yhteensä kolme kappaletta eli pariton määrä, mikä on Hückelin säännön mukainen vaatimus aromaattisuudelle.
Kuva histidiinistä ja selitys sen aromaattisuudesta näkyy alhaalla.

Lähteet
[muokkaa | muokkaa wikitekstiä]- ↑ Amino Acids Vanderbilt University. Viitattu 25.7.2022. (englanniksi)
Aiheesta muualla
[muokkaa | muokkaa wikitekstiä]- Terveysportti: Histidiini
- PubChem: Histidine (englanniksi)
- PubChem: D-Histidine (englanniksi)
- Human Metabolome Database (HMDB): L-Histidine (englanniksi)
- Human Metabolome Database (HMDB): D-Histidine (englanniksi)
- Food Component Database (FooDB): L-Histidine (englanniksi)
- DrugBank: L-Histidine (englanniksi)
- KEGG: L-Histidine (englanniksi)
- KEGG: D-Histidine (englanniksi)
- Small Molecule Pathway Database (SMPDB): Histidine Metabolism, Homo sapiens (englanniksi)
- Small Molecule Pathway Database (SMPDB): Protein Synthesis: Histidine, Homo sapiens (englanniksi)
- ChemBlink: L-Histidine (englanniksi)
- ChemBlink: D-Histidine (englanniksi)
- Liber Herbarum II: Histidiinia sisältäviä kasveja
- Dr. Duke's Phytochemical and Ethnobotanical Databases: Histidine (englanniksi)