Ero sivun ”Käyttäjä:Lahha/karbonyyli” versioiden välillä
→Epäorgaanisia karbonyyli yhdisteitä: <!-- --> ettei näkyisi luokassa |
Ei muokkausyhteenvetoa |
||
| Rivi 1: | Rivi 1: | ||
{{Roskaa|Tarpeeton työversio}} |
|||
[[Image:carbonyl-general.png|150px|thumb|right|Karbonyyli ryhmä(A ja B kuvaa ryhmään liittyneitä atomeja)]] |
[[Image:carbonyl-general.png|150px|thumb|right|Karbonyyli ryhmä(A ja B kuvaa ryhmään liittyneitä atomeja)]] |
||
Versio 5. joulukuuta 2011 kello 08.48
| Tämä käyttäjäsivu on merkitty poistettavaksi välittömästi, koska sen sisältö tai aihe ei sovi tietosanakirjaan tai se on tarpeeton. Perustelut: Tarpeeton työversio Jos olet eri mieltä, kerro mielipiteesi keskustelusivulla. Jos korvaat sivun kelvollisella tai merkintä on mielestäsi ilmeisen virheellinen, poista tämä huomautus ja kerro perustelusi yhteenvedossa tai keskustelusivulla. Älä kuitenkaan poista huomautusta, jos olet itse luonut tämän sivun. Vain ylläpitäjät voivat poistaa sivun. Sivun tyhjentäminen ei vastaa poistamista. Sivujen poistaminen perustuu poistokäytäntöön. Jos artikkelin luoja itse poistaa sivulta tämän merkinnän, lisää hänen keskustelusivulleen koodi: {{subst:Pikapoistomerkintä}} --~~~~. Harkitse myös käyttäjän huomautusmallineen lisäämistä artikkelin luojan keskustelusivulle. Ylläpitäjät: tarkastakaa viittaukset, historia (edellinen) ja lokit ennen poistoa. |

Orgaanisessa kemiassa, karbonyyli ryhmä on funktionaalinen ryhmä, joka koostuu hiili atomista ja happi atomista, jotka ovat kiinnitteneet toisiinsa kaksois-sidokdella
Karbonyyli ryhmä antaa seuraavan tyyppisille yhdisteille teille niiden luonteen(joissa -CO edustaa karbonyyli ryhmää C=O):
->A carbonyl group characterizes the following types of compounds (where -CO denotes a C=O carbonyl group):
| Yhdiste | Aldehydi | Ketoni | Karboksyylihappo | Esteri | Amidi | Enoni | happokloridi | karboksyylihapon anhydridi |
| Rakenne | 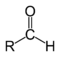 |
 |
 |
 |
 |

| ||
| Rakennekaava | RCHO | RCOR' | RCOOH | RCOOR' | RCONHR' | RC(O)C(R')CR''R''' | RCOCl | (RCO)2O |
Reaktiivisuus
Happi on elektronegatiivisempi kuin hiili, ja siksi vetää elektroneita poispäin nostaakseen sidoksen polaarisuutta. Tästä johtuen karbonyylin hiili atomi tulee elektrofiiliksi, ja reaktiivisemmaksi nukleofiilien kanssa. Myös elektronegatiivinen happi voi reagoida elektrofiilin kanssa. Esimerkiksi protonin kanssa happamassa liuoksessa tai muussa Lewis hapossa.
Alfa vety karbonyyliyhdisteessä on huomattavasti happamampi (noin 1030 kertaa) kuin tavallinen CH sidos. Esimerkiksi asetaldehydin and asetonin pKa-arvot ovat 16.7 ja 19.
Amides are the most stable of the carbonyl couplings due to their high resonance stabilization between the Nitrogen-Carbon and Carbon-Oxygen bonds.
Carbonyl groups can be reduced by reaction with hydride reagents such as NaBH4 and LiAlH4, and by organometallic reagents such as organolithium reagents and Grignard reagents.
Muita tärkeitä reaktioita:
- Wolff-Kishner pelkisyminen
- Clemmensen pelkisyminen
- Muuttuminen thioasetaaliksi
- Hydraatio hemiasetaaliksi ja hemiketaaliksi, ja lopulta asetaaliksi ja ketaaliksi
- Reaktio ammoniakin ja primääristen amiinien kanssa muodostaa imiinejä
- Reaktio hydroksyliamiinin kanssa muodostaa oksiimeja
- Reaktio syanidi anionin kanssa muodostaa syanohydrinejä
- Oxidation with oxaziridines to acyloins
- Reaktio Tebbe's reagent ja phosphonium ylides kanssa muodostaa alkeeneja.
- Perkinsin reaktio
- Tishchenkon reaktio
- Aldolin kondensaatio
- Cannizaron reaktio
α,β-Tyydyttämättömät karbonyyli yhdisteet
α,β-Tyydyttämättömät karbonyyli yhdisteet ovat tärkeä karbonyyli yhdisteiden luokka with the general structure Cβ=Cα−C=O. In these compounds the carbonyl group is conjugated with an alkene (hence the adjective unsaturated), from which they derive special properties. Examples of unsaturated carbonyls are acrolein, mesityl oxide, acrylic acid and maleic acid. Unsaturated carbonyls can be prepared in the laboratory in an aldol reaction and in the Perkin reaction. The carbonyl group, be it an aldehyde or acid, draws electrons away from the alkene and the alkene group in unsaturated carbonyls are therefore deactived towards an electrophile such as bromine or hydrochloric acid. As a general rule with unsymmetric electrophiles hydrogen attaches itself at the α position in an electrophilic addition. On the other hand, these compounds are activated towards nucleophiles in nucleophilic addition.
Spektroskopia
- Infrapuna spektroskopia: C=O sidos absordoi infrapunaa at wavenumbers between approximately 1680–1750 cm−1. This absorption is known as the "carbonyl stretch" when displayed on an infrared absorption spectrum.
- ydinmagneettinen resonanssi: C=O sidos ?exhibits? eri resonansseja ympäröivistä atomeista riippuen. 13C resonanssi karbonyylin hiilellä vaihtelee välillä 160-220 ppm.
- Mass spectrometry
