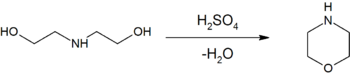Dietanoliamiini
| Dietanoliamiini | |
|---|---|
 |
|
| Tunnisteet | |
| IUPAC-nimi | 2-(2-hydroksietyyliamino)etanoli |
| CAS-numero | |
| PubChem CID | |
| SMILES | C(CO)NCCO [1] |
| Ominaisuudet | |
| Molekyylikaava | C4H11NO2 |
| Moolimassa | 105,138 g/mol |
| Sulamispiste | 28 °C[2] |
| Kiehumispiste | 271 °C[2] |
| Tiheys | 1,097 g/cm3[2] |
| Liukoisuus veteen | Liukenee hyvin veteen |
Dietanoliamiini eli 2,2'-iminodietanoli (C4H11NO2) on alkoholin ja amiinin funktionaaliset ryhmät sisältävä orgaaninen yhdiste. Yhdistettä käytetään muun muassa korroosionestoaineena ja syntetisoitaessa muita kemikaaleja.
Ominaisuudet[muokkaa | muokkaa wikitekstiä]
Dietanoliamiini on huoneenlämpötilassa helposti vetistyviä värittömiä tai valkoisia kiteitä. Ne liukenevat helposti veteen, etanoliin, dietyylieetteriin ja bentseeniin. Yhdisteen vesiliuos on emäksinen. Dietanoliamiini reagoi happojen kanssa muodostaen ensin suoloja, jotka kuumennettaessa muodostavat amideja. Hiilidioksidin kanssa reagoidessaan dietanoliamiini muodostaa karbamaattiyhdisteen.[2][3][4]
Valmistus ja käyttö[muokkaa | muokkaa wikitekstiä]
Dietanoliamiinia valmistetaan etyleenioksidin ja ammoniakin välisellä reaktiolla. Tässä reaktiossa muodostuu dietanoliamiinin lisäksi myös etanoliamiinia ja trietanoliamiinia. Nämä voidaan erottaa toisistaan fraktioivalla tislauksella. Muodostuvien etanoliamiinijohdannaisten suhteeseen voidaan vaikuttaa etyleenioksidin ja ammoniakin määrien suhteella ja kierrättämällä muodostunutta monoetanoliamiinia takaisin reaktoriin.[2][3][4]
Dietanoliamiinia käytetään teollisuussovellutuksissa korroosionestoaineena. Sitä käytetään myös poistamaan hiilidioksidia ja rikkivetyä maakaasun joukosta. Dietanoliamiini on useiden muiden kemikaalien tuotannon lähtöaine. Siitä valmistetaan muun muassa morfoliinia kuumentamalla väkevän rikkihapon kanssa, glyfosaattia, atsiridiinia, pesuaineita, pinta-aktiivisia aineita ja lääkeaineita.[2][3][4]
Lähteet[muokkaa | muokkaa wikitekstiä]
- ↑ Diethanolamine – Substance summary NCBI. Viitattu 14. helmikuuta 2013.
- ↑ a b c d e f Alén, Raimo: Kokoelma orgaanisia yhdisteitä: Ominaisuudet ja käyttökohteet, s. 582. Helsinki: Consalen Consulting, 2009. ISBN 978-952-92-5627-3.
- ↑ a b c Carol Jones, Martha R. Edens & J. Fred Lochary: Alkanolamines from Olefin Oxides and Ammonia, Kirk-Othmer Encyclopedia of Chemical Technology, John Wiley & Sons, New York, 2004. Viitattu 14.02.2013
- ↑ a b c Matthias Frauenkron, Johan-Peter Melder, Günther Ruider, Roland Rossbacher & Hartmut Höke: Ethanolamines and Propanolamines, Ullmann's Encyclopedia of Industrial Chemistry, John Wiley & Sons, New York, 2001. Viitattu 14.02.2013
Aiheesta muualla[muokkaa | muokkaa wikitekstiä]
- Dietanoliamiinin kansainvälinen kemikaalikortti
- Dietanoliamiinin käyttöturvallisuustiedote, Sigma Aldrich, viitattu 18.1.2015.
- Human Metabolome Database (HMDB): Diethanolamine (englanniksi)
- Kyoto Encyclopedia of Genes and Genomes (KEGG): Diethanolamine (englanniksi)
- ChemBlink: Diethanolamine (englanniksi)