Indoksyyli
| Indoksyyli | |
|---|---|
 |
|
 |
|
| Tunnisteet | |
| IUPAC-nimi | 1H-indol-3-oli |
| CAS-numero | |
| PubChem CID | |
| SMILES | C1=CC=C2C(=C1)C(=CN2)O[1] |
| Ominaisuudet | |
| Molekyylikaava | C8H7NO |
| Moolimassa | 133,146 g/mol |
| Sulamispiste | 85 °C[2] |
Indoksyyli eli 3-hydroksi-indoli (C8H7NO) on heterosyklinen aromaattinen yhdiste ja indolin johdannainen. Indoksyyli on oksindolin isomeeri.
Ominaisuudet[muokkaa | muokkaa wikitekstiä]
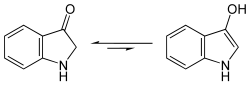
Huoneenlämpötilassa indoksyyli on keltaista kiteistä ainetta, joka liukenee hyvin veteen ja orgaanisiin liuottimiin. Vesiliuoksilla on tyypillinen vihertävänkeltainen fluoresenssi. Yhdisteellä on kaksi tautomerista muotoa enoli- ja ketomuodot. Näistä ketomuoto on stabiilimpi ja tasapainotilassa suurin osa indoksyylistä on ketomuodossa. Indoksyyli on reaktiivinen yhdiste ja hapettuu emäksisissä olosuhteissa helposti indigoksi.[2][3]
Synteesi[muokkaa | muokkaa wikitekstiä]
Indoksyyli valmistetaan synteettisesti antraniilihaposta. Ensimmäisessä vaiheessa antraniilihappo reagoi kloorietikkahapon tai jonkin muun halogeenietikkahapon kanssa. Tämä alkylaatiotuote dekarboksyloidaan emäksen, kuten natriumhydroksidin tai natriumasetaatin avulla. Natriumasetaattia käytettäessä muodostuu indoksyyliasetaattiesteri, joka hydrolysoituu helposti.[3]
Esiintyminen luonnossa ja indigon valmistus[muokkaa | muokkaa wikitekstiä]
Luonnossa indoksyyli muodostaa glukoosin kanssa indikaaniksi kutsutun glykosidin Indigon valmistuksessa indikaani hydrolysoituu indoksyyliksi ja glukoosiksi. Tämän jälkeen reaktiossa muodostuu indoksyyliradikaaleja, jotka dimerisoituvat värittömäksi leukoindigoksi, jonka ilman happi hapettaa indigoksi. Osa indoksyylistä hapettuu näissä olosuhteissa isatiiniksi ja reagoi isatiinin kanssa muodostaen punaista indirubiinia.[4][5]
Lähteet[muokkaa | muokkaa wikitekstiä]
- ↑ Indoxyl – Substance summary NCBI. Viitattu 22. syyskuuta 2013.
- ↑ a b Thomas Scott, Mary Eagleson: Concise encyclopedia chemistry, s. 530. Walter de Gruyter, 1994. ISBN 978-3110114515. Kirja Googlen teoshaussa (viitattu 22.9.2013). (englanniksi)
- ↑ a b John A. Joule,Keith Mills: Heterocyclic chemistry at a glance, s. 94,97. John Wiley & Sons, 2012. ISBN 9781118380215. Kirja Googlen teoshaussa (viitattu 22.9.2013). (englanniksi)
- ↑ Thomas Bechtold,Rita Mussak: Handbook of Natural Colorants, s. 111-114. John Wiley & Sons, 2009. ISBN 978-0-470-74496-3. Kirja Googlen teoshaussa (viitattu 22.9.2013). (englanniksi)
- ↑ Richard L. Myers: The 100 Most Important Chemical Compounds: A Reference Guide, s. 153. Greenwood Press, 2007. ISBN 9780313337581. Kirja Googlen teoshaussa (viitattu 22.9.2013). (englanniksi)
Aiheesta muualla[muokkaa | muokkaa wikitekstiä]
- Human Metabolome Database (HMDB): Indoxyl (englanniksi)
- Kyoto Encyclopedia of Genes and Genomes (KEGG): Indoxyl (englanniksi)
- ChemBlink: 3-Hydroxyindole (englanniksi)
