Ammoniumasetaatti
Siirry navigaatioon
Siirry hakuun
| Ammoniumasetaatti | |
|---|---|
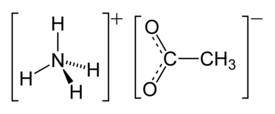 |
|
| Tunnisteet | |
| IUPAC-nimi | ammoniumasetaatti |
| CAS-numero | |
| PubChem CID | |
| SMILES | O=C(O)C.N |
| Ominaisuudet | |
| Molekyylikaava | C2H3O2NH4 |
| Moolimassa | 77,0825 g/mol |
| Sulamispiste | 112 °C (385 K) |
| Kiehumispiste | (purkautuu) |
| Tiheys | 1,07 g/cm3 |
| Liukoisuus veteen | 148 g / 100 ml (4 °C) |
Ammoniumasetaatti on kemiallinen yhdiste, jonka suhdekaava on C2H3O2NH4 ja molekyylikaava CH3COONH4. Se on läpikuultavista rombisista kiteistä koostuvaa väritöntä tai valkoista kiinteää ainetta, jota valmistetaan reagoittamalla ammoniakkia ja etikkahappoa keskenään.
Käyttö ja ominaispiirteet[muokkaa | muokkaa wikitekstiä]
- Ammoniumasetaattia myydään yleisesti kaupallisesti. Ammoniakin asetaattina se on heikon hapon ja heikon emäksen suola, mistä juontuu osa sille ominaisista kemiallisista piirteistä
- Sitä käytetään luonnossa hajoavana yhdisteenä jonkin verran jäänestoaineena.
- Monissa yhteyksissä sitä käytetään etikkahappoon seostettuna. Näin saadaan aikaan puskuriliuos, joka luonnossa hajoaa ionittomiksi osasiksi
- Ammoniumasetaattia voidaan käyttää Knoevenagel-kondensaatiossa orgaaniseen synteesiin [1]
- Sen sulaminen melko alhaisessa lämpötilassa on suolalle suhteellisen harvinainen ominaisuus
- Ammoniumasetaatti on hygroskooppinen yhdiste. Kuumennettaessa se herkästi hajaantuu asetamidiksi ja vedeksi:
- CH3COONH4 → CH3C(O)NH2 + H2O
- Tässä reaktiossa se hajoaa suhteellisen alhaisessa lämpötilassa kahtalaisiksi molekyyleiksi, mikä on suolalle melko harvinaista
- Voidaan käyttää tislatun veden kanssa reagenssina proteiinien saostuksessa
- Käytetään yleisesti massaspektrometriassa vesipuskurina proteiini- ja muiden molekyylien sähkösumutusionisaation (ESI)
- Ammoniumasetaatti on pienissä paineissa haihtuvaa. Tämän takia sitä on käytetty haihtumattomia suoloja sisältävien solupuskurien sijasta valmisteltaessa näytteitä massaspektrometriaan. [2] Haihtuvista suoloista tähän tarkoitukseen on käytetty myös muun muassa ammoniumformiaattia
Lähteet[muokkaa | muokkaa wikitekstiä]
- ↑ G. Jones, Organic Reactions, 1967, volume 15, 204ff (the Knoevenagel Reaction)
- ↑ Berman et al., 2008. J Am Soc Mass Spectrom, 19:1230–1236. (englanniksi)