Vetyperoksidi
| Vetyperoksidi | |
|---|---|
 |
|
 |
|
| Tunnisteet | |
| CAS-numero | |
| PubChem CID | |
| Ominaisuudet | |
| Molekyylikaava | H2O2 |
| Moolimassa | 34,0146 g/mol |
| Ulkomuoto | lievästi sinertävä, liuos väritön |
| Sulamispiste | −0,43 °C (272,72 K) |
| Kiehumispiste | 150,2 °C (423,35 K) |
| Tiheys | 1,4 g/cm3 (neste) |
| Liukoisuus veteen | helposti sekoittuva |
Vetyperoksidi H2O2 on vedyn toinen oksidi, jonka CAS-numero on 7722-84-1. Toinen, tutumpi vedyn oksidi on vesi (H2O).
Ominaisuudet[muokkaa | muokkaa wikitekstiä]
Vetyperoksidi on voimakkaasti hapettava aine. Se hajoaa lämmitettäessä vedeksi ja hapeksi, jolloin prosessissa samalla vapautuu energiaa. Jotkin metallit ja epäpuhtaudet toimivat hajoamisprosessin katalyytteina. Vetyperoksidinestettä voidaan stabiloida muun muassa fosfori-, rikki-, boori- tai sitruunahapolla, asetanilidilla tai asetofenetidiinillä, kun hajoamisprosessia halutaan hidastaa.
Alle 85-prosenttinen vetyperoksidi ei pala, mutta se on voimakkaasti hapettava aine, joten vetyperoksidi yhdessä palavan aineen kanssa aiheuttaa vakavan palamis- tai räjähdysvaaran. Yli 85 %:n vetyperoksidi palaa hajotessaan sinisellä liekillä eli sen hajoamisreaktio on erilainen kuin sitä laimeampien vetyperoksidiliuosten.
Hajotessaan vetyperoksidi muuttuu vedeksi ja hapeksi:
- 2 H2O2 → 2 H2O + O2.
Vetyperoksidi on epästabiili ja hajoaa itsestään, mutta reaktio on erittäin hidas. Reaktiota voi nopeuttaa käyttämällä katalyyttia (esim. mangaanidioksidia). Vetyperoksidissa hapen hapetusluku on -I, hajoamistuotteissa 0 (O2) ja -II (H2O). Reaktiossa siis tapahtuu disproportioituminen, jossa hapetusluku sekä kasvaa että pienenee.
Vetyperoksidin valkaisu- ja desinfiointikyky perustuu hajoamisreaktiossa muodostuvaan erittäin reaktiiviseen vapaaseen happiatomiin.
Toiminta hapettimena ja pelkistimenä[muokkaa | muokkaa wikitekstiä]
Vetyperoksidi toimii tyypillisesti hapettimena happamassa liuoksessa, esimerkiksi
- 2Fe2+ + H2O2 + 2H+ → 2Fe3+ + 2H2O
Se voi toimia myös pelkistimenä emäksisessä liuoksessa:
- 2Fe3+ + H2O2 + 2OH- → 2Fe2+ + 2H2O + O2
Toiminta hapettimena emäksisessä liuoksessa
- Mn(OH)2 + H2O2 → MnO2 + 2H2O
ja pelkistimenä happamassa liuoksessa
- 2Ce4+ + H2O2 → 2Ce3+ + 2H+ + O2
on epätavallista, mutta mahdollista.
Valmistus[muokkaa | muokkaa wikitekstiä]
Vetyperoksidia valmistetaan vedystä ja hapesta 2-etyyliantrakinoni-katalyytillä niin sanotussa Riedl-Pfleiderer–prosessissa:
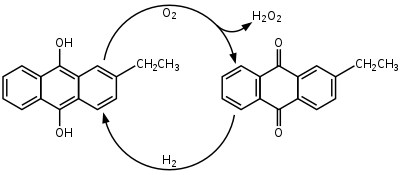
Käyttökohteet[muokkaa | muokkaa wikitekstiä]

Vetyperoksidia on käytetty muun muassa kantorakettien polttoaineen hapettimena.
Teollisuudessa vetyperoksidia käytetään muun muassa sellumassan ja tekstiilien valkaisuun ja desinfiointiaineena lääke- ja elintarviketeollisuudessa. Teollisuuden käyttämässä vetyperoksidissa on yleensä joko 35 tai 50 prosenttia vetyperoksidia, mutta muitakin vahvuuksia on saatavilla.
Uusimmat käyttökohteet vetyperoksidille tulevat olemaan propyleenioksidin uudessa valmistusprosessissa. Tässä prosessissa käytettävät vetyperoksidimäärät ovat erittäin merkittäviä. Kyseinen prosessi onkin merkittävin vetyperoksidin käyttöä lisäävä kohde lähitulevaisuudessa.
Vetyperoksidia voidaan myös käyttää Retrobright-prosessissa, jossa valkaistaan ultraviolettisäteilylle altistunutta kellertäväksi muuttunutta muovia.
Pieninä (alle 5 prosentin) pitoisuuksina vetyperoksidia käytetään kosmetiikassa muun muassa hiustenvalkaisussa, ja esimerkiksi piilolinssien puhdistusliuoksina sekä haavojen desinfioinnissa. Desinfiointikyky perustuu vetyperoksidin hajoamiseen veren toimiessa katalyyttinä. Vapautuva happi tappaa bakteereita.[3][4]
Vetyperoksidia käytetään nykyään melko laajasti, koska sen mahdollinen pääsy ilmaan tai muuten luontoon aiheuttaa vain lyhytaikaista haittaa. Vapaaksi päästyään se hajoaa varsin nopeasti vedeksi ja hapeksi, eikä siten aiheuta pitkäaikaisia ongelmia ympäristölle tai väestölle.
Haitallisuus[muokkaa | muokkaa wikitekstiä]
- 5–8-prosenttiset liuokset luokitellaan ärsyttäviksi aineiksi.
- 8–50-prosenttiset liuokset luokitellaan terveydelle haitallisiksi aineiksi.
- Yli 50-prosenttiset vetyperoksidiliuokset luokitellaan hapettaviksi ja syövyttäviksi aineiksi.
Jatkuva vetyperoksidin käyttö suuvedessä – laimeanakin – saattaa aiheuttaa niin sanotun karvakielen eli kielen filiformisten papillojen liikakasvun.
Joutuessaan kosketuksiin orgaanisen materiaalin – kuten esimerkiksi nahkaisten työkäsineiden – kanssa vetyperoksidi hajoaa voimakkaasti muodostaen samalla lämpöä. Hajoamisreaktiossa muodostuva lämpö ja vapautuva happi aiheuttavat syttymisriskin. Orgaanisen aineen syttyminen on sitä todennäköisempi, mitä suurempi on sen kanssa kosketuksiin joutuneen vetyperoksidin pitoisuus. Syttymisriski voidaan poistaa huuhtelemalla kohdetta runsaalla vedellä.
Katso myös[muokkaa | muokkaa wikitekstiä]
Lähteet[muokkaa | muokkaa wikitekstiä]
- Vetyperoksidin kansainvälinen kemikaalikortti
- Lisätietoja ja turvallisuusohjeita sekä -määräyksiä: (Arkistoitu – Internet Archive)
- Farmakologia ja toksikologia (6. p.), luku Antiseptit ja desinfektioaineet (s. 8/12), kirj. A. Raasmaja ja P. T. Männistö (Arkistoitu – Internet Archive)
Viitteet[muokkaa | muokkaa wikitekstiä]
- ↑ Hydrogen Peroxide (Vetyperoksidi) Käyttöturvallisuustiedote. 25.10.2019. Sigma Aldrich/Merck. Viitattu 28.3.2021.
- ↑ Marilyn Monroen ja Urho Kekkosen salattu yhteys (Arkistoitu – Internet Archive) Helsingin Sanomat 2001
- ↑ Hiusväreissä on voimakkaita kemikaaleja Kuluttajaivirasto
- ↑ Antiseptit ja desinfektioaineet (Arkistoitu – Internet Archive) Medicina
Aiheesta muualla[muokkaa | muokkaa wikitekstiä]
- PubChem: Hydrogen Peroxide (englanniksi)
- Human Metabolome Database: Hydrogen peroxide (englanniksi)
- KEGG: Hydrogen peroxide (englanniksi)
- ChemBlink: Hydrogen peroxide (englanniksi)



