Rikkitetrafluoridi
| Rikkitetrafluoridi | |
|---|---|
 |
|
 |
|
| Tunnisteet | |
| CAS-numero | |
| PubChem CID | |
| Ominaisuudet | |
| Molekyylikaava | SF4 |
| Moolimassa | 108,07 g/mol |
| Ulkomuoto | Väritön kaasu[1] |
| Sulamispiste | -121 °C[2] |
| Kiehumispiste | -40 °C [1] |
| Tiheys | 1,95 g/cm3 (-78 °C)[2] |
| Liukoisuus veteen | Reagoi veden kanssa[1] |
Rikkitetrafluoridi (SF4) on rikin ja fluorin muodostama epäorgaaninen molekyyliyhdiste. Ainetta käytetään pääasiassa orgaanisessa synteesissä valmistettaessa fluorattuja yhdisteitä.
Rakenne[muokkaa | muokkaa wikitekstiä]
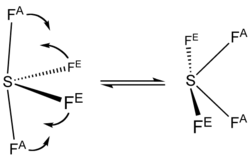
Rikillä on käytettävissään sidoksien muodostumista varten kuusi valenssielektronia. Rikkitetrafluoridissa rikki on sitoutunut neljällä elektronilla, joten sillä on yksi vapaa elektronipari. VSEPR-teorian perusteella yhdisteen avaruusrakenne on hieman vääristynyt trigonaalinen bipyramidi.[3] Rikkiin sitoutuneista fluoriatomeista kaksi on aksiaalisessa asemassa ja kaksi ekvatoriaalisessa asemassa. Kaasufaasissa sidosten pituudet eroavat toisistaan. Aksiaalisen sidoksen pituus on 1,643 Å eli 164,3 nm ja ekvatoriaalisen sidoksen pituus on 1,542 Å eli 164,2 nm. Huoneenlämpötilassa yhdiste on tasapainossa kahden pseudorotaation kautta syntyvän muodon kanssa. Nestemäisenä molekyylit muodostavat välilleen fluorisiltoja.[4]
Ominaisuudet[muokkaa | muokkaa wikitekstiä]
Huoneenlämpötilassa rikkitetrafluoridi on tukahduttavan hajuista väritöntä kaasua. Se reagoi useiden yhdisteiden kanssa ja syövyttää myös lasia. Rikkitetrafluoridi reagoi monien yhdisteiden kanssa, voi toimia myös Lewis-happona ja muodostaa komplekseja. Veden kanssa aine reagoi muodostaen vetyfluoridia ja rikkidioksidia.[4][5]
- SF4 + H2O → 4 HF + SO2
Valmistus[muokkaa | muokkaa wikitekstiä]
Rikkitetrafluoridia voidaan valmistaa rikkidikloridin, kloorin ja natriumfluoridin välisellä reaktiolla 70–80 °C:n lämpötilassa. Liuottimena toimii asetonitriili.[4]
- SCl2 + Cl2 + 4 NaF → SF4 + 4 NaCl
Yhdistettä voidaan valmistaa myös rikkidikloridista ja natriumfluoridista ilman kloorikaasun läsnäoloa. Tällöin reaktio suoritetaan autoklaavissa ja sivutuotteena muodostuu myös dirikkidikloridia.[1]
- 3 SCl2 + 4 NaF → SF4 + S2Cl2 + 4 NaCl
Käyttö[muokkaa | muokkaa wikitekstiä]
Rikkitetrafluoridia käytetään pääasiassa orgaanisessa synteesissä. Alkoholeista muodostuu fluorattuja hiilivetyjä reagoidessaan rikkitetrafluoridin kanssa toisen kertaluvun substituutioreaktiolla. Myös ketonit reagoivat muodostaen difluorideita. Rikkitetrafluoridin etuna on, että tyydyttymättömät yhdisteet pysyvät sillä fluoratessa tyydyttymättöminä. Yhdisteen käytön ongelmana on rikkitetrafluoridin suuri myrkyllisyys ja reaktioiden tulee tapahtua autoklaavissa suuressa paineessa. Tämän vuoksi sen käyttöä on pyritty korvaamaan kehittämällä vähemmän myrkyllisiä johdannaisia kuten dietyyliaminorikkitrifluoridilla.[4][5][6]
Myrkyllisyys[muokkaa | muokkaa wikitekstiä]
Rikkitetrafluoridi on myrkyllistä. Yhdisteen hengittäminen aiheuttaa yskää, hengitysvaikeuksia ja huonoa oloa, johon liittyy oksentelua ja pää- ja kurkkukipua. Yhdiste vaikuttaa samalla tavoin kuin fosgeeni. Joutuessaan iholle tai silmiin yhdiste aiheuttaa syövytysvammoja ja paleltuman.[1][7]
Lähteet[muokkaa | muokkaa wikitekstiä]
- ↑ a b c d e E.M.Karamäki: Epäorgaaniset kemikaalit, s. 159. Kustannusliike Tietoteos, 1983. ISBN 951-9035-61-3.
- ↑ a b Dale L. Perry,Sidney L. Phillips: Handbook of inorganic compounds, s. 393. CRC Press, 1995. ISBN 9780849386718. Kirja Googlen teoshaussa (viitattu 01.06.2010). (englanniksi)
- ↑ Darrell D. Ebbing,Steven D. Gammon: General Chemistry, s. 382. Cengage Learning, 2007. ISBN 978-0618857487. Kirja Googlen teoshaussa (viitattu 01.06.2010). (englanniksi)
- ↑ a b c d Egon Wiberg, Nils Wiberg, Arnold Frederick Holleman: Inorganic chemistry, s. 527. Academic Press, 2001. ISBN 978-0-12-352651-9. Kirja Googlen teoshaussa (viitattu 01.06.2010). (englanniksi)
- ↑ a b Catherine E. Housecroft,A. G. Sharpe: Inorganic chemistry, s. 509. Pearson Education, 2007. ISBN 9780131755536. Kirja Googlen teoshaussa (viitattu 01.06.2010). (englanniksi)
- ↑ Peer Kirsch: Modern fluoroorganic chemistry: synthesis, reactivity, applications, s. 60. Wiley-VCH, 2007. ISBN 978-3-527-30691-6. Kirja Googlen teoshaussa (viitattu 01.06.2010). (englanniksi)
- ↑ Rikkitetrafluoridin kansainvälinen kemikaalikortti Viitattu 01.06.2010}