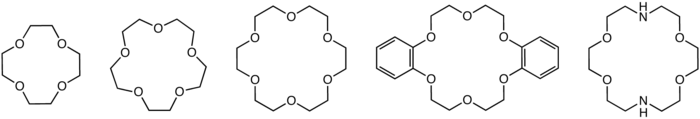
Kruunueetterit

Kruunueetteri on heterosyklinen yhdiste, joka sisältää useita eetteriryhmiä [1]. Kruunueetterit nimesi Charles J. Pedersen niiden kruunua muistuttavan rakenteen vuoksi. Kruunueetterit voivat sulkea sisäänsä metalli-ioneja erittäin selektiivisesti[2] eli ne sitoutuvat vain tiettyyn ioniin eivätkä muodosta sidosta muiden metalli-ionien kanssa. Yleisimpiä kruunueettereitä voidaan pitää etyleenioksidin oligomeereinä. Kruunueettereitä voidaan käyttää ionoforeina eli ionien kuljettajina[2] esimerkiksi vedestä kloroformiin [3]
Historiaa[muokkaa | muokkaa wikitekstiä]
Vuonna 1967 Charles Pedersen, työskennellesään DuPontilla, löysi yksinkertaisen synteesin etsiessään ainetta, joka pystyisi kationien kelaatioon. Hän liitti katekolimolekyylejä toisiinsa hydroksyyliryhmien välityksellä. Yllätyksekseen Pedersen huomasi, että eräs kuusi happiatomia sisältävä rengasmainen sivutuote [2] kykeni muodostamaan vahvan sidoksen kaliumioniin. Myöhemmin Pedersen tutki erityisesti dibentsokruunueettereitä.
Selektiivisyys[muokkaa | muokkaa wikitekstiä]
Kruunueetterin happiatomilla on yksi sitoutumaton elektronipari, niillä se muodostaa koordinaatiosidoksen metallikationin kanssa. Selektiivisyys riippuu suuresti kruunueetterin koosta. Mikäli metalli-ioni on säteeltään liian suuri, se ei kykene pääsemään kruunueetterirenkaan sisälle, eikä sidosta muodostu. Vastaavasti liian pieni kationi on liian kaukana happiatomeista eikä tehokas sidoksen muodostaminen onnistu [1]. Kruunueetterit toimivat siis Lewis-emäksinä[4].
Kruunueetterijohdannaisia[muokkaa | muokkaa wikitekstiä]
Bentsokruunueetterit[muokkaa | muokkaa wikitekstiä]
Bentsokruunueettereissä kruunueetterimolekyyliin on liittynyt yksi tai usein kaksi bentseenirengasta. Bentsokruunueettereitä käytetään muodostamaan komplekseja ioniyhdisteiden kanssa . Bentsokruunueetterit ovat myrkyllisiä [5].
Atsakruunueetterit[muokkaa | muokkaa wikitekstiä]
Atsakruunueettereissä yksi tai useampi happiatomeista on korvattu typpiatomilla, joka voi muodostaa metalli-ionin kanssa kolme sidosta. Kaksi- ja useampisyklisiä atsakruunueettereitä kutsutaan kryptandeiksi [1].
Lariaattiset kruunueetterit[muokkaa | muokkaa wikitekstiä]
Lariaattisen kruunueetterin runkona on atsakruunu, jonka yhteen typpiatomiin on liittynyt hiilivetyhäntä, jossa on eetteriryhmä. Substraatti muodostaa sidoksen hännän kanssa ja hiilivetyketju taipuessaan asettaa metalli-ionin atsakruunurenkaan sisälle [1]. Yleensä kruunueetterit muodostavat sidoksia pääasiassa alkali- ja maa-alkalimetalli-ionien välillä, mutta lariaattiset kruunueetterit voivat sitoutua myös muidenkin metallien, kuten hopean ja lyijyn, kanssa [6]. Lariaattisten kruunueettereiden häntä voi myös olla vastaanottaa protoneja. Tämä vaikuttaa myös aineen selektiivisyyteen[7]. Lariaattiset kruunueetterit ovat myös huomattavan tehokkaita ionoforeja [3][6]
Lähteet[muokkaa | muokkaa wikitekstiä]
- ↑ a b c d Philip Ball suom. Kimmo Pietiläinen: Kemian eturintamassa:Matka molekyylien maailmaan. Vaasa: Terra Cognita, 1997.
- ↑ a b c What is a Crown Ether? DuPont. Arkistoitu 23.6.2008. Viitattu 11. heinäkuuta 2008.
- ↑ a b Synthesis and complexation properties of some novel lariat-crown ethers Cat.inist. Viitattu 11. heinäkuuta 2008. [vanhentunut linkki]
- ↑ Crown Ethers University of Calgary. Viitattu 11. heinäkuuta 2008.
- ↑ Macrosyclic polyethers: Dibentzo-18-crown-6 polyether and dicyclohexyl-18-crown-6 polyether Organic Syntheses. Viitattu 11. heinäkuuta 2008.
- ↑ a b New Ag+- and Pb2+-selective electrodes with lariat crown ethers as ionophores Cat.insist. Viitattu 11. heinäkuuta 2008. [vanhentunut linkki]
- ↑ Metal ion complexation and separation by crown ether compounds Texas Tech University Libraries. Arkistoitu 17.5.2008. Viitattu 11. heinäkuuta 2008.
Aiheesta muualla[muokkaa | muokkaa wikitekstiä]
 Kuvia tai muita tiedostoja aiheesta Kruunueetterit Wikimedia Commonsissa
Kuvia tai muita tiedostoja aiheesta Kruunueetterit Wikimedia Commonsissa