Ero sivun ”Vetyfluoridi” versioiden välillä
| [katsottu versio] | [katsottu versio] |
p r2.6.5) (Botti lisäsi: ms:Hidrogen florida |
|||
| Rivi 36: | Rivi 36: | ||
[[Luokka:Fluoridit]] |
[[Luokka:Fluoridit]] |
||
[[Luokka:Epäorgaaniset hapot]] |
[[Luokka:Epäorgaaniset hapot]] |
||
[[ar:فلوريد الهيدروجين]] |
|||
[[ms:Hidrogen florida]] |
|||
[[bs:Fluorovodonik]] |
|||
[[bg:Флуороводород]] |
|||
[[ca:Fluorur d'hidrogen]] |
|||
[[cs:Fluorovodík]] |
|||
[[de:Fluorwasserstoff]] |
|||
[[el:Υδροφθόριο]] |
|||
[[en:Hydrogen fluoride]] |
|||
[[fa:هیدروژن فلوئورید]] |
|||
[[fr:Fluorure d'hydrogène]] |
|||
[[ko:플루오린화 수소]] |
|||
[[hy:Ֆտորաջրածին]] |
|||
[[hr:Fluorovodik]] |
|||
[[lv:Fluorūdeņradis]] |
|||
[[hu:Hidrogén-fluorid]] |
|||
[[nl:Waterstoffluoride]] |
|||
[[ja:フッ化水素]] |
|||
[[no:Flussyre]] |
|||
[[nn:Flussyre]] |
|||
[[pl:Fluorowodór]] |
|||
[[ru:Фтороводород]] |
|||
[[simple:Hydrogen fluoride]] |
|||
[[sk:Fluorovodík]] |
|||
[[sr:Fluorovodonik]] |
|||
[[sh:Fluorovodonik]] |
|||
[[sv:Vätefluorid]] |
|||
[[uk:Фтороводень]] |
|||
[[zh:氟化氢]] |
|||
Versio 14. maaliskuuta 2013 kello 18.02
| Vetyfluoridi | |
|---|---|
[[Tiedosto: |275px|]] |275px|]] |
|
| Tunnisteet | |
| Muut nimet | Fluorivety, Fluorivetyhappo |
| CAS-numero | |
| PubChem CID | |
| Ominaisuudet | |
| Molekyylikaava | HF |
| Moolimassa | 20,008 g/mol |
| Ulkomuoto | Väritön neste tai kaasu |
| Sulamispiste | −84 °C (189,15 K) |
| Kiehumispiste | 19.54 °C (292,69 K) |
| Tiheys | 0.922 kg/m3 |
| Liukoisuus veteen | Erittäin hyvä |
Vetyfluoridi eli fluorivety (HF) on vedyn ja fluorin muodostama molekyyliyhdiste. Muista halideista poiketen vetyfluoridin kiehumispiste on hyvin lähellä huoneen lämpötilaa. Vetyfluoridin vesiliuosta kutsutaan fluorivetyhapoksi, joka on vain heikosti hapan, mutta vahvasti korrodoiva. Ainetta käytetään laajasti petrokemianteollisuudessa, ja se on tärkeä yhdiste niin kutsuttujen superhappojen valmistuksessa.
Vetyfluoridin rakenne
Vetyfluoridikiteet koostuvat siksakmaisista molekyyliketjuista. Molekyylien sisäiset kovalenttiset sidokset ovat noin 95 pikometriä pitkiä. Molekyylit ovat kiinni toisissaan sähköisellä vetovoimalla, vetysidoksilla. (Merkitty kuvaan katkoviivoilla.)
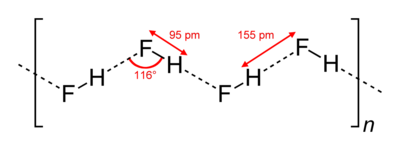
Myös nestemäisessä olomuodossa vetyfluoridimolekyylit muodostavat ketjuja, tosin lyhyempiä, noin viiden tai kuuden molekyylin mittaisia. Vetyfluoridin korkeampi kiehumispiste muihin halideihin verrattuna johtuu pitkälti vahvoista vetysidoksista.
Käyttö ja valmistus
Vetyfluoridia käytetään muun muassa polymeerien fluorauksessa, maaöljyn jalostuksessa, lasinvalmistuksessa ja etsauksessa, alumiinin tuotannossa ja uraaniheksafluoridin syntetisoinnissa. Vetyfluoridin vesiliuos myös syövyttää oksideja, joten sitä käytetään teräksen valmistuksessa ja puolijohdeteollisuudessa piin epäpuhtauksien poistossa.
Vetyfluoridia valmistetaan kalsiumfluoridista ja rikkihaposta.
- CaF2 + H2SO4 → CaSO4 + 2 HF
Ainetta myydään yleensä anhydridinä tai 70- tai 49-prosenttisina vesiliuoksina eli fluorivetyhappona. Voimakkaan reaktiivisuutensa ja syövyttävyytensä takia vetyfluoridia ja sen vesiliuosta säilytetään yleensä teflon-astioissa. Fluori ei reagoi teflonin kanssa, joka itse on fluoriyhdiste.
Terveysvaikutukset
Aine on myrkyllistä ja voi olla jopa kuolettavaa pieninäkin annoksina ravinnossa tai ihon läpi imeytyneenä. Iholle joutuessaan aine voi aiheuttaa vakavia vaurioita ja hengitettynä tai nieltynä pahoinvointia.[1]