Ioninen neste
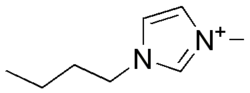
Ioninen neste eli suolasula on neste, joka koostuu ioneista, yleensä orgaanisesta kationista ja epäorgaanisesta, moniatomisesta anionista. Tyypillisesti kationi on varsin suuri epäsymmetrinen molekyyli, esimerkiksi kvaternäärinen ammonium-, imidatsoli-, pyridiini- ja fosfoniumjohdannainen. Nykyisin yleisin ionisissa nesteissä esiintyvä kationi on 1-butyyli-3-metyyli-imidatsoliumioni (bmim). Anioneina käytetään yleensä "neutraaleja" heikosti koordinoituvia anioneja, kuten heksafluorofosfaattia PF6−, tetrafluoroboraattia BF4−, bis(trifluorometyylisulfonyyli)amidia (F3CSO2)2N− ja trifluorimetaanisulfonaattia F3CSO3−. Ensimmäinen valmistettu ioninen neste oli etyyliammoniumnitraatti C2H5NH3+ NO3−, s.p. 12 °C), joka löydettiin vuonna 1914.[1] Ionisilla nesteillä on useita edullisia ominaisuuksia, jonka vuoksi niitä voidaan käyttää monissa teollisissa sovellutuksissa. Ionisilla nesteillä on erittäin alhainen höyrynpaine, ts. ne eivät haihdu. Niillä on laaja nestemäisen olomuodon lämpötila-alue, parhaimmillaan −96 – +400 °C. Ioniset nesteet eivät ole paloherkkiä toisin kuin monet orgaaniset liuottimet. Eräät ioniset nesteet ovat niukkaliukoisia sekä veteen että orgaanisiin liuottimiin, jolloin ioniseen nesteeseen liuenneet yhdisteet voidaan helposti uuttaa erilleen ja ioninen neste voidaan käyttää uudelleen. Haihtumattomuutensa ja kierrätettävyytensä vuoksi ionisia nesteitä pidetään ympäristöystävällisenä vaihtoehtona perinteisille orgaanisille liuottimille. Ionisilla nesteillä on erinomaiset liuotusominaisuudet ja kemialliset reaktiot tapahtuvat niissä nopeammin kuin perinteisissä liuottimissa. Lisäksi niillä on myös katalyyttisiä ominaisuuksia. Erityisesti kaksifaasireaktiossa, Diels–Alder-reaktioissa ja Friedel–Crafts-reaktioissa ioniset nesteet ovat osoittautuneet erittäin käyttökelpoisiksi. Esimerkiksi Friedel–Crafts-reaktio voidaan tehdä ionisessa nesteessä ilman Lewishappo-katalyyttiä. Ioniset nesteet ovat hyviä liuottimina myös mikroaalto- ja entsyymireaktiossa[2]. Ionisissa nesteissä voidaan käyttää homogeenisia (liukenevia) katalyyttejä, jolloin arvokas katalyytti voidaan ottaa talteen ja kierrättää.
Lähteet[muokkaa | muokkaa wikitekstiä]
- F. Endres, S. Zein El Abedin (2006). "Air and water stable ionic liquids in physical chemistry". Phys. Chem. Chem. Phys. 8: 2101. doi:10.1039/b600519p.
- S. Fujita, H. Kanamaru, H. Senboku and M. Arai (2006). "Preparation of Cyclic Urethanes from Amino Alcohols and Carbon Dioxide Using Ionic Liquid Catalysts with Alkali Metal Promoters" (open access). Int. J. Mol. Sci. 2006 (7): 438–450.
Viitteet[muokkaa | muokkaa wikitekstiä]
- ↑ P. Walden, Bull. Acad. Sci. St. Petersburg 1914, 405–422
- ↑ Adam J. Walker & Neil C. Bruce: Cofactor-dependent enzyme catalysis in functionalized ionic solvents. Chemical Communications, 2004, nro 22. doi:10.1039/b410467f. (englanniksi)
Aiheesta muualla[muokkaa | muokkaa wikitekstiä]
- Jyri-Pekka Mikkolan aliokirjoitus: Ioniset nesteet - tavoitteena uuden ajan vihreä kemia Turun Sanomat. 6.2.2005.
