Laktoperoksidaasi
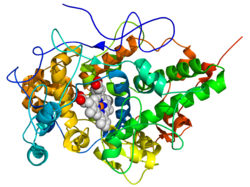
Laktoperoksidaasi on entsyymi, joka hapettaa useita inorgaanisia ja orgaanisia substraatteja vetyperoksidin avulla. Sitä esiintyy useiden nisäkkäiden maidossa, syljessä ja kyynelissä, joissa se toimii antibakteerisena aineena.
Rakenne ja toiminta[muokkaa | muokkaa wikitekstiä]
Laktoperoksidaasi on molekyylimassaltaan 78 kDa oleva entsyymi ja on glykoproteiini. Yhdiste vaatii toimiakseen koentsyymikseen hemiryhmän ja kalsiumioneja. Laktoperoksidaasi on emäksinen entsyymi ja sen isoelektrinen piste on 9–10. Lehmän maidossa laktoperoksidaasin pitoisuus on 30 mg/l. Laktoperoksidaasi on aktiivinen erityisesti gramnegatiivisia bakteereja vastaan. Sen antibakteeriset ominaisuudet perustuvat sen kykyyn hapettaa tiosyanaatti-ioneja hypotiosyanaateiksi, bromideja hypobromiiteiksi ja jodideja hypojodiiteiksi. Hapettimena entsyymi käyttää vetyperoksidia, joka pelkistyy vedeksi. Nämä hapettumistuotteet ovat hyvin reaktiivisia ja aiheuttavat soluseinän rikkoutumisen. Tämä estää bakteerien kasvun tai tappaa ne. Laktoperoksidaasilla on tärkeä rooli maidon säilymisessä. Entsyymi hapettaa myös useita orgaanisia yhdisteitä esimerkiksi fenoleja. Entsyymi denaturoituu kuumennettaessa yli 70 °C:n lämpötilaan, mutta sietää hyvin happamia olosuhteita ja proteolysoivien entsyymien vaikutusta.[1][2][3][4][5][6][7]
Laktoperoksidaasi voidaan erottaa maidosta käyttämällä kationisia eli positiivisesti varautuneita ioninvaihtohartseja. Entsyymiä voidaan lisätä suuvesiin ja hammastahnoihin bakteereja tappavaksi aineeksi sekä piilolinssien puhdistusnesteisiin.[6]
Lähteet[muokkaa | muokkaa wikitekstiä]
- ↑ Rolf Jost: Milk and Dairy Products, Ullmann's Encyclopedia of Industrial Chemistry, John Wiley & Sons, New York, 2007. Viitattu 11.4.2016
- ↑ Charlotte Horsmans Poulsen, Karsten M. Kragh, Jens Frisbak Sorensen, Catherine Grassin, Marga Herweijer, Jan Wilms, André de Roos & Jorn Borch Soe: Enzymes, 3. Food Application, Ullmann's Encyclopedia of Industrial Chemistry, John Wiley & Sons, New York, 2008. Viitattu 11.4.2016
- ↑ Nicholas J. Russell,Grahame W. Gould: Food Preservatives, s. 276. Springer, 2012. ISBN 978-0-306-47736-2. Kirja Googlen teoshaussa (viitattu 11.4.2016). (englanniksi)
- ↑ Young W. Park: Bioactive Components in Milk and Dairy Products, s. 169. John Wiley & Sons, 2009. ISBN 978-0-8138-1949-5. Kirja Googlen teoshaussa (viitattu 11.4.2016). (englanniksi)
- ↑ Young W. Park,George F. W. Haenlein: Handbook of Milk of Non-Bovine Mammals, s. 322. John Wiley & Sons, 2008. ISBN 978-0-470-99972-1. Kirja Googlen teoshaussa (viitattu 11.4.2016). (englanniksi)
- ↑ a b Zeynep Ustunol: Applied Food Protein Chemistry, s. 447. John Wiley & Sons, 2014. ISBN 9781118860595. Kirja Googlen teoshaussa (viitattu 11.4.2016). (englanniksi)
- ↑ Y. H. Hui,Frank Sherkat: Handbook of Food Science, Technology, and Engineering, s. 27–28. CRC Press, 2005. ISBN 9781466507876. Kirja Googlen teoshaussa (viitattu 11.4.2016). (englanniksi)