Osmoosi
| Tätä artikkelia tai sen osaa on pyydetty parannettavaksi, koska se ei täytä Wikipedian laatuvaatimuksia. Voit auttaa Wikipediaa parantamalla artikkelia tai merkitsemällä ongelmat tarkemmin. Lisää tietoa saattaa olla keskustelusivulla. Tarkennus: artikkeliin voisi lisätä yleistajuista sisältöä. Osio "diffuusion mallinnus" on ymmärrettävä vain korkeakoulutasolla |
Osmoosi on liuottimen diffuusiota puoliläpäisevän kalvon läpi. Osmoosissa liuotin (yleensä vesi) siirtyy kalvon läpi, mutta kalvo ei päästä läpi liuottimeen liuenneita aineita. Liuotin siirtyy sille puolelle, jolla liuenneen aineen pitoisuus on suurempi. Jos esimerkiksi puoliläpäisevä kalvo erottaa suolaisen veden ja vähemmän suolaisen veden oheisen kuvan osoittamalla tavalla, vettä siirtyy makeamman veden osasta suolaisen veden osan puolelle.

Diffuusion mallinnus[muokkaa | muokkaa wikitekstiä]
Diffuusio-liikkeen suunta ja vauhti riippuvat
- veden konsentraatiosta kalvon eri puolilla
- painegradientista ja
- painovoimasta.
Yllä olevat tekijät yhdessä määrittävät kemiallisen potentiaaligradientin vedelle kalvon yli. Osmoosille pätee sama termodynaaminen sääntö kuin diffuusiollekin: veden liike on suuremmasta potentiaali(energia)tilasta pienempään.
Käytännössä määritellään vesipotentiaali (), joka saadaan jakamalla kemiallinen potentiaali (J mol-1) veden osittaisella molaarisella tilavuudella (1 mooli vettä vastaa m3 mol-1.) Vesipotentiaali on periaatteessa sama asia, kuin veden Gibbsin vapaa energia per yksikkötilavuus, ja se mitataan J m-3 (= Pa).
Formaalisesti ( on suhteellinen käsite. Se mitataan suhteessa puhtaaseen veteen merenpinnalla standardilämpötilassa ja paineessa) missä:
- on liuenneen aineen potentiaali (katso osmoottinen paine) ja kuvaa liuenneen aineen vaikutusta veden potentiaaliin. Yleisesti jonkun aineen liukeneminen veteen vähentää veden vapaata energiaa laimentamalla sitä (entropia kasvaa koska liuenneet molekyylit kasvattavat järjestelmän epäjärjestäytyneisyyttä). Puhtaan veden konsentraatio on n. 56 mol dm-3. Liuottamalla aineita veteen vähentää siis , tehden siitä negatiivisen verrattuna pelkän veden arvoon . Laimeille liuoksille vedessä hajoamattomille yhdisteille (kuten glukoosi) noudattaa van't Hoffin yhtälöä:
- missä cs on liuenneen aineen konsentraatio (mol dm-3), R kaasuvakio ja T absoluuttinen lämpötila. Jos kyseessä on hajoava aine, yhtälön oikea puoli kerrotaan hajoamisesta seuraavien hiukkasten määrällä (kerroin olisi esimerkiksi 2 NaCl:lle).
- on painepotentiaali, joka kuvaa (positiivisen tai negatiivisen) paineen vaikutusta veden potentiaaliin. Tällä on yleensä merkitystä vasta 5 metrissä (ja sitä korkeammalla). Negatiivinen paine vähentää veden potentiaalia (vähemmän energiaa, potentiaali pienenee), ja positiivinen paine kasvattaa sitä (enemmän energiaa, potentiaali kasvaa). Paine mitataan suhteessa merenpintaan. Tämä komponentti on tärkeä soluseinällisissä soluissa. Protoplasti puskee periksiantamatonta soluseinää vasten ja Newtonin kolmannen lain mukaan seinä puskee takaisin samalla voimalla. Tämä johtaa siihen, että esimerkiksi kasvit eivät nuupahda kasaan.
- on painovoiman vaikutukset sisällyttävä termi.
Osmoosi on siis veden liikettä suuremmasta vesipotentiaalista pienempään potentiaaliin () puoliläpäisevän kalvon ylitse.
Osmoosi biologisissa järjestelmissä[muokkaa | muokkaa wikitekstiä]
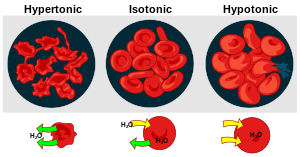
Soluseinättömissä soluissa solukalvon ylitse ei ole merkittävää paine- tai painovoimaeroa. Vesipotentiaaliero riippuu siis pelkästään :stä, joka puolestaan riippuu liuenneiden aineiden konsentraatioista. Esimerkiksi punasolut ovat herkkiä osmoottiselle veden liikkeelle. Isotonisessa liuoksessa solun ulkopuolinen konsentraatio vastaa solun sisäistä, jolloin punasolut ovat normaalissa kaarevassa muodossaan (kts. kuva).
Hypotonisessa liuoksessa solun sisällä on suurempi konsentraatio (, missä on solunsisäinen ja solun ulkopuolinen), jolloin (eli solun sisällä on negatiivisempi , kuin sen ulkopuolella) ja vesi syöksyy soluun. Tämä johtaa solun pullistumiseen, joka voi johtaa jopa solun kokonaisvaltaiseen repeytymiseen. Tullessaan soluun vesi tasapainottaa konsentraatioeroja, ja solun paisuminen jatkuu, kunnes potentiaalit ovat yhtäsuuruiset. Hypertonisessa liuoksessa tilanne on päinvastainen ja vesi pakenee solusta. Välttääkseen mahdollisesti vahingolliset veden liikkeet, solut aktiivisesti pumppaavat ioneja solukalvon ylitse (mm. Na+, K+ ja Cl-) säädelläkseen konsentraatioeroja.
Soluseinällisissä soluissa hypotonisessa liuoksessa soluseinä vastustaa laajenemista johtaen paineeseen. Tämä johtaa kasvuun, joka kasvaa, kunnes solunsisäinen on sama, kuin solun ulkopuolinen. Hypertonisessa liuoksessa tilanne on päinvastainen: vesi poistuu solusta, kunnes . Vesi jatkaa poistumistaan, kunnes solun tilavuus on pienentynyt tarpeeksi, jotta on tasapainottanut solunsisäisen :n vastaamaan solunulkopuolista. Tämä johtaa usein solukalvon kuoriutumiseen pois soluseinältä, eli plasmolyysiin. Myös soluseinälliset solut pumppaavat ioneja (pääasiassa H+) estääkseen radikaalit veden liikkeestä johtuvat muutokset.
Soluseinällisen solun kasvu vaatii myös soluseinän rakenteen löysentämistä. Solu laskee sisäistä laskemalla :tä pumppaamalla sisään veteen liuenneita aineita. Tämä johtaa veden sisääntuloon, ja sitä kautta :n kasvuun (paineen kasvuun), joka työntää soluseinän uuteen laajempaan muotoon. Jotkut antibiootit heikentävät bakteereiden soluseiniä, pienentäen niiden kykyä sietää sisäistä painetta johtaen bakteerisolujen hajoamiseen.
Osmoottinen mekanismi[muokkaa | muokkaa wikitekstiä]
Vesi pystyy ylittämään solukalvot ilman huomattavia ongelmia huolimatta veden pienestä rasvojen läpäisykyvystä. Solukalvoilla onkin niin kutsuttuja akvaporiini-proteiineja (engl. aquaporins), joiden rakenteessa on n. 400 nm suuruinen reikä, joka mahdollistaa veden liikkeen. Solu reguloi akvaporiineja fosforyloinnilla ja solunsisäisellä Ca2+:n konsentraatiolla. Nykytietämyksen mukaan osmoosi on yhdistelmä yksittäisten vesimolekyylien diffuusiota solukalvon lävitse, sekä suurten määrien liikettä avointen akvaporiinien läpi.
Osmoosi energiantuotannossa[muokkaa | muokkaa wikitekstiä]
Statkraft Norjassa on rakentanut maailman ensimmäisen pilottiluonteisen osmoosivoimalaitoksen, jonka toiminta alkoi 24. marraskuuta 2009.[1] Ensimmäinen täysikokoinen kaupallinen laitos voisi olla toiminnassa vuonna 2015. Osmoosivoimalaitos käyttää meriveden ja makean jokiveden välistä painetta uusiutuvana energianlähteenään.[2] [3]
Katso myös[muokkaa | muokkaa wikitekstiä]
Lähteet[muokkaa | muokkaa wikitekstiä]
- ↑ Maailman ensimmäinen osmoosivoimala starttasi Norjassa Tietokone.fi 27.11.2009.
- ↑ Norja rakentaa maailman ensimmäisen osmoosivoimalaitoksen YLE 3.10.2007
- ↑ Osmoottisen paineen simulointi online















