Litiumdi-isopropyyliamidi
| Litiumdi-isopropyyliamidi | |
|---|---|
 |
|
| Tunnisteet | |
| IUPAC-nimi | Litiumdi(propan-2-yyli)atsanidi |
| CAS-numero | |
| PubChem CID | |
| SMILES | [Li+].CC(C)[N-]C(C)C[1] |
| Ominaisuudet | |
| Molekyylikaava | C6H14NLi |
| Moolimassa | 107,123 g/mol |
| Tiheys | 0,79 g/cm3 |
| Liukoisuus veteen | Reagoi veden kanssa |
Litiumdi-isopropyyliamidi eli LDA (C6H14NLi) on di-isopropyyliamiinin litiumsuola. Yhdiste on erittäin vahvasti emäksinen ja sitä käytetään orgaanisissa synteeseissä.
Ominaisuudet[muokkaa | muokkaa wikitekstiä]
Huoneenlämpötilassa litiumdi-isopropyyli on suhteellisen epästabiili aine, joka hajoaa ilman kosteuden vaikutuksesta. Yhdiste liukenee poolittomiin orgaanisiin liuottimiin kuten pentaaniin ja heksaaniin, mutta polymerisoituu hitaasti muodostaen liukenemattoman polymeerin. Litiumdi-isopropyyliamidi liukenee paremmin eettereihin, mutta reagoi tetrahydrofuraania lukuun ottamatta niiden kanssa. Usein ainetta käytetään heksaaniliuoksena, jossa on mukana pieni määrä tetrahydrofuraania. Litiumdi-isopropyyliamiini on vahvasti emäksinen. Sen pKa-arvo tetrahydrofuraanissa on 35.[2][3][4]
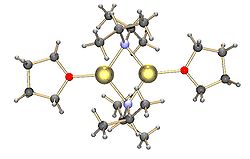
Röntgenkristallografiaan perustuen litiumdi-isopropyyliamidi on kiinteänä dimeeri. Se muodostaa myös dimeerejä liuoksissa esimerkiksi tetrahydrofuraanin kanssa.[5]
Valmistus ja käyttö[muokkaa | muokkaa wikitekstiä]
Litiumdi-isopropyyliamidia voidaan valmistaa di-isopropyyliamiinin ja n-butyylilitiumin välisellä reaktiolla.[2][3] Toinen tapa, joka soveltuu erityisesti suureen mittakaavaan on litiumin reaktio styreenin kanssa ja tämä yhdiste reagoi di-isopropyyliamiinin kanssa dietyylieetteriliuoksessa.[3]
Litiumdi-isopropyyliamidi on erittäin vahva emäs, jota käytetään yleisesti orgaanisessa kemiassa enolaattien ja allyylisten, aromaattisten ja heteroaromaattisten karbanionien valmistamiseen, koska se kykenee poistamaan happaman protonin jopa hiileltä. Yhdisteen etuna on se, että se ei useista muista emäksistä poiketen ole nukleofiilinen. Tämä johtuu siitä, että isopropyyliatomit aiheuttavat steeristä estettä negatiivisen typpiatomin ympärille, eikä se pääse reagoimaan nukleofiilina. Litiumdi-isopropyyliamidia hyödynnetään muun muassa useiden lääkeaineiden, kuten gemfibrotsiilin, synteeseissä.[2][3][4]
Lähteet[muokkaa | muokkaa wikitekstiä]
- ↑ Diisopropylamine – Substance summary PubChem. NCBI. Viitattu 31.3.2014.
- ↑ a b c Ulrich Wietelmann & Martin Steinbild: ,Lithium and Lithium Compounds Ullmann's Encyclopedia of Industrial Chemistry, John Wiley & Sons, New York, 2014. Viitattu 31.3.2014
- ↑ a b c d Wouter I. Iwema Bakker, Poh Lee Wong, Victor Snieckus, Jeffrey M. Warrington & Louis Barriault: Lithium Diisopropylamide, e-EROS Encyclopedia of Reagents for Organic Synthesis, John Wiley & Sons, New York, 2004. Teoksen verkkoversio Viitattu 31.3.2014
- ↑ a b Jonathan Clayden, Nick Greeves, Stuart Warren: Organic Chemistry, s. 467. Oxford University Press, 2012. ISBN 978-0-19-927029-3. (englanniksi)
- ↑ Michael B. Smith & Jerry March: March's Advanced Organic Chemistry, s. 389. John Wiley & Sons, 2007. ISBN 978-0-471-72091-1. (englanniksi)