DMMDA

| |
DMMDA
| |
| Systemaattinen (IUPAC) nimi | |
| 1-(4,7-Dimetoksi-1,3-bentsodioksoli-5-yyli)propaan-2-amiini | |
| Tunnisteet | |
| CAS-numero | |
| ATC-koodi | ? |
| PubChem CID | ? |
| Kemialliset tiedot | |
| Kaava | C12H19NO4 |
| Moolimassa | 241,287 g/mol |
| Fysikaaliset tiedot | |
| Sulamispiste | 170–175 °C |
| Farmakokineettiset tiedot | |
| Hyötyosuus | ? |
| Metabolia | ? |
| Puoliintumisaika | ? |
| Ekskreetio | ? |
| Terapeuttiset näkökohdat | |
| Raskauskategoria |
? |
| Reseptiluokitus |
|
| Antotapa | nieltynä |
DMMDA eli 2,5-dimetoksi-3,4-metyleenidioksiamfetamiini on vähemmän tunnettu psykedeelinen muuntohuume. Alexander Shulgin kuvailee DMMDA:n synteesiä ja vaikutuksia kirjassaan PiHKAL.[1]
Vaikutukset[muokkaa | muokkaa wikitekstiä]
Alexander Shulgin kuvailee DMMDA:n vaikutusten olevan pahoinvointi, mydriaasi, ataksia, visuaaliset hallusinaatiot, ajan hidastuminen ja depersonalisaatio.[1] Shulginin mukaan yksi annos DMMDA:ta on 30–75 mg ja sen vaikutukset kestävät 6–8 tuntia.[1] Shulgin väittää 75 mg suuruisen annoksen vastaavan 75–100 μg suuruista annosta LSD:tä.[1]
Kemia[muokkaa | muokkaa wikitekstiä]
Kemiallisesti katsottuna DMMDA on 4-substituoitu-2,5-dimetoksiamfetamiini eli niin sanottu DOx-yhdiste.[1] Shulgin kommentoi kirjassaan, että samoin kuin TMA:lla DMMDA:lla on ainakin teoriassa 6 eri isomeeria.[1] Toistaiseksi DMMDA-2 on ainoa toinen näistä isomeereista, jota on syntetisoitu.[1] Teoriassa Crowea exalata ja Crowea angustifolia var. angustifolia kasvilajien kasviöljyn sisältämästä eksalatasiinistä eli 1-allyyli-2,6-dimetoksi-3,4-metyleenidioksibentseenistä voisi valmistaa DMMDA:n kolmannen isomeerin.[2]
Synteesi[muokkaa | muokkaa wikitekstiä]
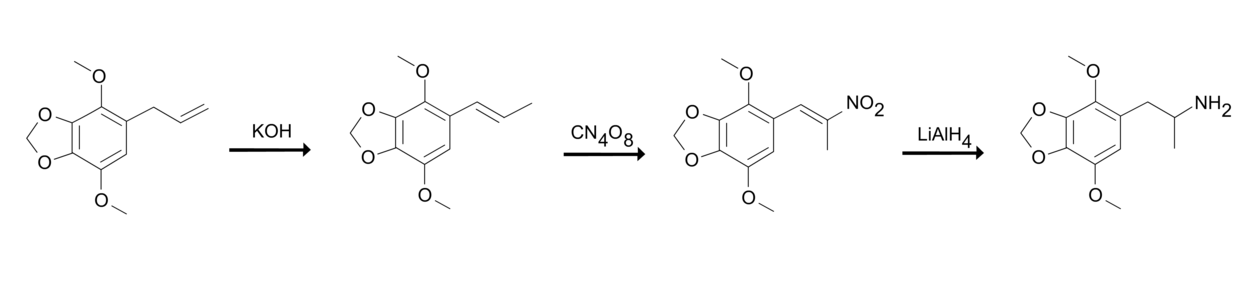
Alexander Shulgin kuvailee PiHKAL-kirjassaan yhtä tapaa syntetisoida DMMDA:ta käyttäen prekursorina apiolia eli 1-allyyli-2,5-dimetoksi-3,4-metyleenidioksibentseeniä.[1] Aluksi apioli eristetään persiljan kasviöljystä jakotislaamalla.[1] Apioli haihtuu 165–167:n celsiusasteen lämpötilassa ja 27:n elohopeamillimetrin paineessa.[1] Sitten apiolia kohdistetaan isomerisaatioreaktioon lisäämällä se etanoliseen kaliumhydroksidiliuokseen ja lämmittämällä liuosta. Isomerisaation johdosta syntyy isoapiolia eli 2,5-dimetoksi-3,4-metyleenidioksi-1-propenyylibentseeniä; apiolin sisältämä kahden hiilen välinen kaksoissidos vaihtaa paikkaa muodostaen isoapiolia.[1] Sitten isoapioli kohdistetaan nitraukseen tetranitrometaanin avulla jääkylvyn lämpötilassa pyridiinin tehdessä reaktioseoksesta emäksisen, minkä johdosta syntyy 2-nitro-isoapiolia eli 1-(2,3-dimetoksi-3,4-metyleenidioksifenyyli)-2-nitropropeenia.[1] 2-Nitro-isoapioli pelkistetään sitten DMMDA:n vapaaemäsmuotoon. 2-Nitro-isoapioli lisätään siis dietyylieetterin ja litiumalumiinihydridin liuokseen refluksointiolosuhteissa ja inertin eli reaktiokyvyttömän kaasun (kuten esimerkiksi heliumin) alla.[1] Lopulta DMMDA:n vapaaemäsmuoto muutetaan DMMDA hydrokloridiksi.[1]
-
Alexander Shulginin kehittämä DMMDA:n synteesi apiolista.
Shulginin kehittämä DMMDA:n synteesi ei ole kovin turvallinen, koska se sisältää muun muassa tetranitrometaanin käyttöä. Tetranitrometaani on myrkyllinen, karsinogeeninen ja helposti räjähtävä aine.[3] DMMDA:ta voi valmistaa myös esimerkiksi DMMDP2P:n eli 2,5-dimetoksi-3,4-metyleenidioksifenyylipropan-2-onin avulla. DMMDP2P:tä voi valmistaa apiolista esimerkiksi kohdistamalla se Wacker-hapetukseen p-Bentsokinonin kanssa. DMMDP2P:tä voi myös valmistaa isomerisoimalla apioli isoapioliksi, kohdistamalla se peretikka-hapetukseen ja lopulta hydrolyyttiseen dehydraukseen.[4] Sitten lopulta DMMDP2P voidaan kohdistaa pelkistävään aminointiin ammoniumkloridin ja natriumsyanoboorihydridin kanssa, jonka johdosta syntyy DMMDA:ta.[5]
Laki[muokkaa | muokkaa wikitekstiä]
DMMDA:ta ei ole toistaiseksi luokiteltu Suomessa kuluttajamarkkinoilta kielletyksi psykoaktiiviseksi aineeksi.[6]
Lähteet[muokkaa | muokkaa wikitekstiä]
- ↑ a b c d e f g h i j k l m n Alexander Shulgin: Pihkal: A Chemical Love Story. Transform Press, 1991. ISBN 0-9630096-0-5.
- ↑ "Essential oils of the genus Crowea (Rutaceae)." (July 1997). Journal of Essential Oil Research 9 (4): 401–409. doi:.
- ↑ National Toxicology Program: Tetranitromethane Report On Carcinogens. National Toxicology Program.
- ↑ "Chemical markers from the peracid oxidation of isosafrole" (Heinäkuu 2008). Forensic Science International 179 (1): 44–53. doi:. PMID 18508215.
- ↑ "Centrally active N-substituted analogs of 3,4-methylenedioxyphenylisopropylamine (3,4-methylenedioxyamphetamine)" (Helmikuu 1980). Journal of Pharmaceutical Sciences 69 (2): 192–195. doi:. PMID 6102141.
- ↑ Valtioneuvoston asetus kuluttajamarkkinoilta kielletyistä psykoaktiivisista aineista finlex.fi.