Ohutkerroskromatografia

Ohutkerroskromatografia eli ohutlevykromatografia (usein käytetään myös lyhennettä TLC, engl. Thin layer chromatography) on kromatografiamenetelmä, joka perustuu siihen, että tutkittava näyte kiinnitetään kiinteään faasiin (kromatografialevyyn) ja annetaan liikkuvan faasin (liuottimen) nousta sitä pitkin kapillaarivoimien avulla. Tutkittava seos liikkuu kromatografialevyn huokoisessa materiaalissa liuottimen eli eluentin tai ajoliuoksen avulla. Eri yhdisteet liikkuvat eri nopeuksilla johtuen niiden erilaisista vuorovaikutuksista liuottimen ja kromatografialevyn kanssa, jolloin ne erottuvat toisistaan. Ohutkerroskromatografian hyviä ominaisuuksia ovat erityisesti helppo toteutettavuus, huokea hinta, nopeus ja hyvä erotuskyky. Tämän vuoksi se on yksi käytetyimmistä kromatografisista menetelmistä seosten komponenttien määrittämiseen ja reaktioiden seurantaan.
Historia
[muokkaa | muokkaa wikitekstiä]Ohutkerroskromatografian historian voidaan katsoa alkaneeksi 1800-luvun loppupuolella. Alankomaalainen biologi M. W. Beijerinck tutki vuonna 1889 suolahappo- ja rikkihappoliuosten kulkeutumista ohuella gelatiinikerroksella ja huomasi niiden liikkuvan eri nopeuksilla. Suolahapon tunnistamiseksi hän lisäsi gelatiiniin hopeanitraattia ja rikkihapon tunnistamiseksi bariumkloridia. Toinen alankomaalainen biologi H. P. Wijsman kehitti Beijerinckin menetelmää ja käytti tutkimuksissaan analyyttien havaitsemiseen fluoresoivaa bakteerikantaa gelatiinikerroksessa. Tällä tavoin hän osoitti vuonna 1898, että maltaan diastaasi oli kaksi eri entsyymiä. Varsinaisesti ohutkerroskromatografian ensimmäisinä kehittäjinä pidetään kuitenkin Izmailovia ja Shraiberia, jotka vuonna 1938 esittivät idean käyttää komponenttien erottamiseen kiinteälle pinnalle sidottua adsorbenttia.[1][2][3][4]
Yhdysvaltalaiset J. E. Meinhard ja N. F. Hall kehittivät vuonna 1949 tekniikan, jossa he käyttivät seliittiä (piimaata) sitomaan alumiinioksidia kiinteällä levylle. Tätä tekniikkaa he käyttivät erottamaan toisistaan muun muassa metallikationeja ja eteerisiä öljyjä. 1950- ja 1960-lukujen aikana Justus G. Kirchner kehitti ohutkerroskromatografian tekniikoita ja esitteli muun muassa kaksiulotteisen ohutkerroskromatografian ja menetelmiä ohutkerroskromatografian käyttämiseen reaktioiden seurantaan. Menetelmän yleistymisen kannalta merkittävää työtä teki Stahl 1950-luvun lopulla, kun hän kehitti helpon levyjen pinnoitusmenetelmän ja osoitti, että TLC:n avulla avulla voitiin helposti suorittaa useita erilaisia erotuksia. Kaupalliset pinnoitetut kromatografialevyt ilmestyivät vuonna 1961.[1][2][3][4][5]
Uusimmat menetelmän kehityskohteista liittyvät kiraalisten molekyylien enantiomeerien erottamiseen toisistaan. Tämä perustuu erityiseen syklodekstriinipinnoitteeseen. Menetelmää on tutkittu muun muassa lääkeaineiden biologisesti aktiivisten enantiomeerien erottamiseen tehottomista isomeereista, käänteisfaasitekniikoihin ja stationäärifaasiseoksia sisältäviin ohutkerroskromatografialevyihin.[1][2][4]
Erottumisen perusteet
[muokkaa | muokkaa wikitekstiä]Kuten muissakin kromatografisissa menetelmissä, komponenttien erottuminen perustuu seoksen yhdisteiden, paikallaan olevan faasin eli stationäärifaasin ja liikkuvan faasin, jota kutsutaan myös ajoliuokseksi tai eluentiksi, välisiin vuorovaikutuksiin. Komponentit liikkuvat stationäärifaasin pinnalla eri nopeuksilla. Nopeuserot johtuvat komponenttien ja faasien välisistä Van der Waalsin voimista, dipoli-dipolivuorovaikutuksista, molekyylien välisistä vetysidoksista ja kemisorptiosta. Stationäärifaasi on tyypillisesti polaarinen silikageeli- tai alumiinioksidikerros. Tällöin polaariset yhdisteet kulkeutuvat liikkuvan faasin mukana lyhyemmän matkan samassa ajassa kuin poolittomammat (rasvaliukoisemmat) yhdisteet. Polaarisempaa liuotinta käytettäessä myös poolisten (vesiliukoisten) yhdisteiden kulkemat matkat pitenevät.[6][7]
Ohutkerroskromatografia muistuttaa siis toiminnaltaan paperikromatografiaa. Erona on vain se, että kiinteänä faasina ohutkerroskromatografiassa toimii paperin sijasta hienojakoinen jauhe, kuten selluloosa tai silikageeli. Jauhe tai geeli on sidottu tasaisena, ohuena kerroksena esimerkiksi lasi-, muovi- tai alumiinilevyn pintaan.[6]
Tärkeä suure ohutkerroskromatografiassa on retentiota kuvaava Rf-arvo, joka määritellään seuraavasti[6]:
Tämän perusteella komponentti voidaan tunnistaa, mutta Rf-arvo ei ole komponentin absoluuttinen arvo, vaan riippuu ajoliuoksen koostumuksesta, lämpötilasta ja ajoastian koosta. Arvo vaihtelee 0–0,999 välillä. Tyypillisesti liuotinsysteemin valinnalla arvoksi pyritään saamaan 0,2–0,4.[6][8][9][10]
Kahden eri komponentin erottumista toisistaan kuvaa resoluutio Rs, joka määritellään kahden eri aineen täplän keskipisteen välisen matkan x ja täplien keskimääräisen halkaisijan suhteena. Jos arvo on 1, ovat komponentit erottuneet toisistaan melko hyvin.[9]:
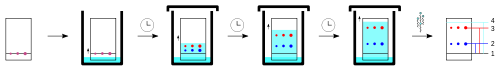
Alla olevassa kuvasarjassa on esitetty vihreiden lehtien eri värikomponenttien erottuminen ohutlevykerroskromatografiassa.
-
Vaihe 1
-
Vaihe 2
-
Vaihe 3
-
Vaihe 4
-
Vaihe 5
-
Vaihe 6
-
Vaihe 7
Stationäärifaasimateriaalit
[muokkaa | muokkaa wikitekstiä]Yleisin stationäärifaasi ohutkerroskromatografiassa on silikageeli, joka valmistetaan levyn pinnalle hydrolysoimalla polypiihappoja emäksisellä tai happamalla liuoksella. Kerroksen paksuus on tyypillisesti 0,25 millimetriä ja hiukkaskoko 5–25 mikrometriä. Korkean suorituskyvyn ohutkerroskromatografiassa eli HPTLC:ssä hiukkaskoko on pienempi kuin tavallisessa ohutlevykromatografiassa. Silikageeli on hivenen hapanta. Silikageelin joukkoon voidaan lisätä apuaineita, kuten sinkkisilikaattia, joka fluoresoi, kun sitä valaistaan UV-valolla, jonka aallonpituus on 254 nanometriä. Näytetäplät näkyvät tummina fluoresoivalla levyllä.[11][12][13]
Alumiinioksidi on hieman emäksistä, joten emäksiset yhdisteet kulkeutuvat ja erottuvat siinä paremmin kuin silikageelilevyillä. Alumiinioksidi adsorboi orgaanisia yhdisteitä melko voimakkaasti. Se adsorboi myös vettä, joten levyt usein aktivoidaan ennen käyttöä 125–150 °C:n lämpötilassa, jolloin vesi poistuu ja adsorptiopaikat vapautuvat.[11][12][13]
Piimaa eli seliitti on fossiloituneiden piilevien jauhettua kuorta. Se on hyvin hienojakoista, mutta adsorptiokyky on melko heikko. Tyypillisesti sitä käytetään yhdessä muiden adsorbenttimateriaalien kanssa stationäärifaasina.[12][13]
Mikrokiteistä tai jauhettua selluloosaa voidaan käyttää myös stationäärifaasina. Parhaiten selluloosaa stationäärifaasinaan sisältävät ohutkerroskromatografialevyt soveltuvat hydrofiilisten yhdisteiden, kuten sokereiden ja aminohappojen, erottamiseen. Selluloosa voi olla myös muunneltua, kuten karboksimetyyli-, dietyyliaminoetyyli- tai polyetyleeni-imiiniselluloosaa.[12][13]
Polyamidien, kuten polykaprolaktaamin ja Nylon 6.6:n, käyttö stationäärifaasina on yleistynyt. Niillä muuten heikosti erottuvat fenolit erottuvat hyvin. Näitä levyjä käytettäessä myös vesi sopii ajoliuokseksi.[12][13]
Ohutkerroskromatografia voidaan suorittaa myös käänteisfaasikromatografiana, jolloin stationäärifaasi on pooliton (rasvaliukoinen) ja eluentti poolinen (vesiliukoinen). Nämä levyt sisältävät stationäärifaasinaan silikaa, joka on tehty sisältämään poolittomia silyylieetteriryhmiä käsittelemällä sitä diklooridimetyylisilaanilla.[12][13]
Hyvin valikoivia ohutkerroskromatografialevyjä ovat ioninvaihtokerroksen tai syklodekstriiniä sisältävät levyt. Ioninvaihtostationäärifaasi sopii hyvin sekä orgaaniseen että epäorgaaniseen faasiin. Syklodekstriini on rengasmainen molekyyli, jonka onkaloon toinen enantiomeereista pidättyy paremmin kuin toinen ja näin ne erottuvat. Menetelmää käytetään erityisesti lääkeaineiden optisen puhtauden varmistamiseen.[12][13]
Eluenttisysteemit
[muokkaa | muokkaa wikitekstiä]Eluentin eli liuottimen valinta on ohutlevykerroskromatografiassa tärkeää, koska se vaikuttaa suuresti komponenttien erottumiseen ja käytössä on suuri määrä erilaisia liuottimia ja niiden seoksia. Polaaristen (vesiliukoisten) yhdisteiden erottamiseen käytetään vahvasti polaarisia ajoliuoksia, kun poolittomille (rasvaliukoisille) yhdisteille myös pooliton liuotin on yleensä paras vaihtoehto. Yleisliuottimena ohutkerroskromatografiassa käytetään dikloorimetaania tai etyyliasetaattia. Muita usein käytettyjä ajoliuoksia ovat metanoli, heksaani ja petrolieetteri sekä näiden seokset eri suhteissa, joissa on pooliton ja polaarisempi komponentti.[6][13][14]
Eluentin vahvuutta kuvaava parametri E0 kuvaa ajoliuoksen adsorptioenergiaa adsorbenttiyksikköä kohden. Mitä suurempi arvo on, sitä suurempia ovat myös komponenttien Rf-arvot. E0-arvot ovat suurempia poolisilla kuin poolittomilla eluenteilla. Voimakkailla eluenteilla Rf-arvot ovat suurempia kuin heikommilla liuottimilla, mutta myös erottuminen voi olla huonompaa. Resoluutio voi parantua, jos käytetään proottisia ajoliuoksia, jotka voivat muodostaa vetysidoksia. Jos näyte liikkuu levyllä huonosti, käytetään polaarisempaa ajoliuosta ja jos Rf-arvo on liian suuri, lisätään ajoliuokseen poolitonta liuotinta tai vaihdetaan koko ajoliuos poolittomampaan.[6][13]
Suorittaminen
[muokkaa | muokkaa wikitekstiä]Ohutkerroskromatografia suoritetaan eli ajetaan sille tarkoitetussa, tyypillisesti lasisessa, astiassa. Näyte lisätään ohuella kapillaariputkella noin viisi senttimetriä korkealle levylle hieman alareunan yläpuolelle ja levy asetetaan astiaan, jonka pohjalla on eluenttikerros. Astiassa voidaan käyttää suodatinpaperia eluentin höyrynpaineen tasaamiseksi. Eluentin annetaan nousta levyä pitkin ylös, minkä jälkeen levy visualisoidaan.[11][10]
Levy voi olla myös pyöreä, jolloin kromatografia suoritetaan sitä varten kehitetyssä laitteistossa. Näyte lisätään levylle ja eluentti kulkee joko keskeltä reunoille tai reunoilta keskelle, jolloin komponentit erottuvat rengasmaisina vyöhykkeinä.[15]
Kaksiulotteinen ohutkerroskromatografia
[muokkaa | muokkaa wikitekstiä]Kaksiulotteisessa ohutkerroskromatografiassa ensimmäinen ajo suoritetaan normaalisti ja komponentit erottuvat pystysuorassa suunnassa. Tämän jälkeen eluentin annetaan haihtua levyltä ja suoritetaan toinen ajo asettaen tällä kertaa levy poikittain ajoastiaan. Näin saadaan tietoa esimerkiksi näytekomponenttien mahdollisesta hajoamisesta kromatografian suorituksen aikana. Toinen ajo voidaan suorittaa myös eri eluentissa tai levylle voidaan lisätä vertailuyhdisteitä ennen toista ajoa.[6][15]
Käänteisfaasimenetelmä
[muokkaa | muokkaa wikitekstiä]Ohutkerroskromatografiaa voidaan suorittaa myös käänteisfaasikromatografiana. Siinä stationäärifaasi on pooliton ja eluentti poolinen. Käänteisfaasikromatografian etuna ovat normaaliin ohutkerroskromatografiaan verrattuna parempi valikoivuus, parempi polaarittomien yhdisteiden erottuminen, helpompi näytteen puhdistus ja levyn aktivoinnin tarpeettomuus.[12]
Täplien havainnointi
[muokkaa | muokkaa wikitekstiä]Erityisesti orgaaniset yhdisteet ovat usein värittömiä, joten niiden paikantamiseksi TLC-levyllä täytyy käyttää havaitsemiskeinoja, jotka voidaan jakaa kahteen ryhmään, näytettä tuhoamattomiin ja analyytin kanssa tapahtuvaan reaktioon perustuviin menetelmiin. Näytettä voidaan tutkia UV-valon alla, jolloin eräät yhdisteet fluoresoivat. Tyypillisimmät UV-lampun intensiteettimaksimit ovat aallonpituuksilla 254 ja 366 nanometriä. Jodilla värjäys voi olla analyytistä riippuen joko sitä tuhoamaton tai sen kanssa reagoiva. Jodivärjäyksessä kromatografialevy asetetaan kammioon, jossa on jodihöyryä. Orgaaniset yhdisteet absorboivat jodia voimakkaammin kuin levy ja näkyvät tummanruskeina täplinä vaaleamman ruskealla levyllä. Jos jodi ei ole reagoinut analyytin kanssa, voidaan käyttää myös muita valikoivampia värjäysmenetelmiä, kun jodi on haihdutettu levyltä.[11][15][16]
Komponenttien havaitsemiseen voidaan käyttää myös värjäysreagensseja, jotka reagoivat analyytin kanssa muodostaen värillisen yhdisteen.[11][15] Alla olevassa taulukossa on esitetty yleisimmin käytettyjä värjäysaineita.
| Reagenssi | Värjäytyvät yhdisteet[11][16][17] | Väri [11][16][17] |
|---|---|---|
| Kaliumpermanganaatti | Yleisreagenssi, erityisesti helposti hapettuvat yhdisteet kuten alkoholit ja tyydyttymättömät yhdisteet, myös ketonit, aldehydit ja esterit | Keltainen |
| Vanilliini | Useat yhdisteet | Eri värejä |
| Fosfomolybdeenihappo | Erityisesti helposti hapettuvat yhdisteet | Sinivihreä |
| Ammoniumceriummolybdaatti | Yleisreagenssi, valikoivampi kuin fosfomolybdeenihappo | Sininen |
| Anisaldehydi | Yleisreagenssi, alkeenit ja alkyynit eivät värjäydy | Useita eri värejä |
| Ninhydriini | Amiinit | Keltainen tai punainen |
| 2,4-dinitrofenyylihydratsiini | Aldehydit ja ketonit | Keltainen tai oranssi |
Sovelluksia
[muokkaa | muokkaa wikitekstiä]Epäorgaaninen analyysi
[muokkaa | muokkaa wikitekstiä]Ohutkerroskromatografiaa käytetään epäorgaanisessa analytiikassa erottamaan erityisesti metallikationeja seoksesta. Ensimmäisenä tähän tarkoitukseen menetelmää käyttivät Meinhard ja Hall, jotka erottivat näin rauta- ja sinkkikationeja seoksesta. Menetelmää käytetään muun muassa kivi-, maaperä-, teollisuus- ja jätevesinäytteiden tutkimiseen. Myös metallien läsnäoloa biologisissa näytteissä ja lääkeaineissa voidaan tutkia.[3]
Orgaaninen analyysi
[muokkaa | muokkaa wikitekstiä]Orgaanisessa analyysissä ohutlevykromatografiaa käytetään useisiin eri tarkoituksiin. Tärkeimmät ovat seoksessa olevien komponenttein määrän selvittäminen, analyytin puhtauden määrittäminen ja reaktioiden seuranta. Ohutkerroskromatografialla voidaan esimerkiksi määrittää, onko näyte riittävän puhdasta herkempää kaasukromatografia- tai HPLC-analyysiä varten.[14]
Reaktioiden seuranta käyttäen ohutkerroskromatografiaa
[muokkaa | muokkaa wikitekstiä]Ohutkerroskromatografiaa käytetään usein erityisesti orgaanisten reaktioiden etenemisen seuraamiseen. TLC-levylle asetetaan ohuella kapillaarilla kolme täplää: yksi täplä on reaktiota rajoittavalle lähtöaineelle, toinen lähtöaineen ja reaktioseoksen niin kutsuttu ”co-spot” ja kolmas reaktioseoksesta otettava näyte. Jos ohutkerroskromatografian ajon jälkeen levyllä ei erotu reaktioseoksesta otetussa näytteessä lähtöaineen täplää, on reaktio päättynyt.[18][19]
Muita reaktionseurantatekniikoita
[muokkaa | muokkaa wikitekstiä]Ohutkerroskromatografia on nopea ja helppo tekniikka orgaanisten reaktioiden seurantaan, mutta muita menetelmiä käytetään yha enemmissä määrin. Kaikki yhdisteet eivät erotu kovin hyvin ohutkerroskromatografialla ja tällöin käytetään yleensä HPLC-laitteistoa tai helposti haihtuvilla yhdisteillä kaasukromatografiaa. HPLC on hitaampi menetelmä kuin ohutkerroskromatografia, mutta kaasukromatografia on lähes yhtä nopea. Näiden etuna on myös se, että niitä voidaan käyttää myös kvantitatiivisen analyysiin eli määrittämään tuotteiden konsentraatioita näytteissä. Hyvin pienen mittakaavan reaktioissa edistymisen seurantaan voidaan käyttää myös NMR-spektrometriä.[20]
Ohutkerroskromatografia verrattuna muihin kromatografiatekniikoihin
[muokkaa | muokkaa wikitekstiä]Ohutkerroskromatografian etuja ovat helppo tekniikka, jossa ei vaadita erikoislaitteistoja, helppo näytteenkäsittely, menetelmän nopeus, halvat käyttökustannukset, pieni näytemäärän tarve ja vähäinen liuottimien kulutus. Paperikromatografiaan verrattuna menetelmä on nopeampi ja erotuskyvyltään parempi. Kaasukromatografia ja HPLC ovat ohutkerroskromatografiaa parempia erotuskyvyltään ja vähemmän alttiita olosuhteiden vaikutuksille ja niissä on helpommin mahdollisuus kvantitatiiviseen analyysiin. Ne vaativat kuitenkin huomattavasti kalliimpia laitteistoja.[20][3][12]
Katso myös
[muokkaa | muokkaa wikitekstiä]Lähteet
[muokkaa | muokkaa wikitekstiä]- J. Leonard, B. Lygo & G. Procter: Advanced Practical Organic Chemistry. Taylor & Francis, 1998. ISBN 0-7487-4071-6. (englanniksi)
- A. Braithwaite,F. J. Smith: Chromatographic methods. Springer, 1996. ISBN 978-0-7514-0158-5. Kirja Googlen teoshaussa. (englanniksi)
- Ali Mohammad: ”21. Inorganic and Organometallic Compounds”, Handbook of Thin-Layer Chromatography. CRCPress, 2003. ISBN 978-0824748661. Kirja Googlen teoshaussa. (englanniksi)
- Kimberly S. Cleaves & Mark S. Lesney: Capitalizing on Chromathography. Enterprize of Chemical Sciences, 2005, s. 75–79. American Chemical Society. Artikkelin verkkoversio (PDF). (englanniksi)
- Joseph Sherma & Gertrud Morlock: Capitalizing on Chromatography. Journal of Planar Chromatography, 2008, 21. vsk, nro 6, s. 75–79. American Chemical Society. doi:10.1556/JPC.21.2008.6.15. (englanniksi)
- Joseph C. Touchstone: Thin layer chromatography, Ullmann's Encyclopedia of Industrial Chemistry, John Wiley & Sons, New York, 2002. ISBN 978-3527306732. DOI:10.1002/14356007.b05_301. Teoksen verkkoversio
- John C. Gilbert,Stephen F. Martin: Experimental Organic Chemistry. Cengage Learning, 2010. ISBN 978-1439049143. Kirja Googlen teoshaussa. (englanniksi)
- Jerry R. Mohrig, Christina Noring Hammond & Paul F. Schatz: Techniques in Organic Chemistry. W. H. Freeman, 2006. ISBN 978-0716769354. Teoksen verkkoversio. (englanniksi) (Arkistoitu – Internet Archive)
Viitteet
[muokkaa | muokkaa wikitekstiä]- ↑ a b c Braithwaite & Smith, s. 44–45
- ↑ a b c Cleaves & Lesney, s. 75–76
- ↑ a b c d Mohammad, s. 793
- ↑ a b c Sherma & Morlock, s. 471
- ↑ Touchstone, s. 1
- ↑ a b c d e f g Leonard, Lygo & Procter, s. 149–151
- ↑ Braithwaite & Smith, s. 49
- ↑ Braithwaite & Smith, s. 46
- ↑ a b Mohammad, s. 794
- ↑ a b Mitä on TLC eli ohutlevykromatografia? Virtuaalilaboratorio. Teknillinen korkeakoulu, Orgaanisen kemian laboratorio. Viitattu 15.5.2011.
- ↑ a b c d e f g Leonard, Lygo & Procter, s. 146–149
- ↑ a b c d e f g h i Braithwaite & Smith, s. 51–59
- ↑ a b c d e f g h i Touchstone, s. 2–4, 8–10
- ↑ a b Mohrig, Hammond, Schatz, s. 307, 347–351
- ↑ a b c d Touchstone, s. 13–16
- ↑ a b c Värjäyrsreagenssit Virtuaalilaboratorio. Teknillinen korkeakoulu, Orgaanisen kemian laboratorio. Viitattu 14.5.2011.
- ↑ a b Thin Layer Chromatography stains REACH Devises. Viitattu 15.5.2011. (englanniksi)
- ↑ Gilbert & Martin, s. 184
- ↑ Thin Layer Chromatography (TLC) Notes. University of Rochester. Arkistoitu 11.7.2011. Viitattu 15.5.2011. (englanniksi)
- ↑ a b Leonard, Lygo & Procter, s. 153, 158, 232
Aiheesta muualla
[muokkaa | muokkaa wikitekstiä] Kuvia tai muita tiedostoja aiheesta Ohutkerroskromatografia Wikimedia Commonsissa
Kuvia tai muita tiedostoja aiheesta Ohutkerroskromatografia Wikimedia Commonsissa






