Typpioksidisyntaasi
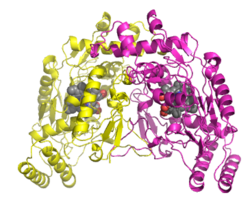
Typpioksidisyntaasi eli NOS on entsyymi, joka katalysoi typpioksidin muodostumista arginiinista. Typpioksidin lisäksi reaktiossa muodostuu sitrulliinia. Typpioksidi on tärkeä aine soluissa signaalienvälitysprosesseissa, minkä vuoksi myös typpioksidisyntaasilla on suuri merkitys tässä tehtävässä. Lisäksi entsyymillä on osuus tulehdusreaktioissa. Typpioksidisyntaasin EC-numero on EC 1.14.13.39 ja entsyymiä esiintyy sekä eukaryootti- että bakteerisoluissa.[1][2][3]
Rakenne ja toiminta[muokkaa | muokkaa wikitekstiä]
Typpioksidisyntaasi on suurikokoinen proteiini ja molekyylimassaltaan noin 130–150 kDa. Ihmisellä esiintyy kolme typpioksidisyntaasin isoentsyymiä, jotka ovat neuronaalinen typpioksidisyntaasi (nNOS), joka esiintyy aivoissa ja hermosoluissa, endoteelisoluissa esiintyvä endoteelinen typpioksidisyntaasi (eNOS) ja ihmisen elimistön puolustusreaktioissa bakteereita vastaan, haavan parantumisessa ja tulehduksissa esiintyvä indusoituva typpioksidisyntaasi (iNOS). Indusoituvaa typpioksidisyntaasia esiintyy useissa soluissa kuten hepatosyyteissä, makrofageissa, monosyyteissä ja neutrofiileissä. Näistä nNOS ja iNOS ovat rakenteeltaan dimeerejä, jotka koostuvat reduktaasi- ja oksidaasialayksiköistä, joita yhdistää kalmoduliiniin sitoutuva yksikkö, Kun kalmoduliini sioutuu proteiiniin, muuttuu entsyymin rakenne siten, että hapetus-pelkistysreaktiohin osallistuvat alayksiköt tulevat lähemmäksi toisiaan. Endoteelinen typpioksidisyntetaasi on sitoutunut solukalvoon myristoylaation seurauksena.[1][3][4][5][6][7][8]
Typpioksidisyntaasin kaikki isoentsyymimuodot ovat sikäli poikkeuksellisia entsyymejä, että ne tarvitsevat peräti viisi koentsyymiä, kalmoduliinin, NADPH-molekyylin, FAD-molekyylin, FMN-molekyylin, hemiryhmän ja tetrahydrobiopteriinin. Kalmoduliini osallistuu entsyymin toiminann säätelyyn ja NADPH, FAD, FMN ja hemiryhmä osallistuvat elektroninsiirtoreaktioihin.[1][3][4][7][8] Lisäksi typpioksidisyntaasin nNOS- ja eNOS-isoentsyymit tarvitsevat toimiakseen kalsiumioneja, jotka sitoutuvat kalmoduliiniin[4][5].
Typpioksidisyntaasin katalysoiman reaktion ensimmäisessä vaiheessa elektronit siirtyvät NADPH:lta arginiinille, josta muodostuu N-ω-hydroksiarginiinia. Tämä yhdiste hapettuu edelleen NADPH:n avulla hapen läsnä ollessa sitrulliiniksi ja samalla vapautuu typpioksidia.[2] Reaktion sivutuotteena voi muodostua superoksideita[1].
Typpioksidisyntaasia inhiboivat arginiinia rakenteellisesti muistuttavat yhdisteet kuten agmatiini, kanavaniini ja metyyliarginiini[1]. Lisäksi entsyymiä iniboivat kalmoduliinin antagonistit[3]. Entsyymin inhibiittoreita on tutkittu aivojen iskemian ehkäisyssä ja metyyliarginiinia on tutkittu verenmyrkytysten hoitoon, mutta tutkimukset keskeytettiin kolmanteen faasiin.[3][5]
Lähteet[muokkaa | muokkaa wikitekstiä]
- ↑ a b c d e EC 1.14.13.39 - nitric-oxide synthase (NADPH dependent) Brenda. Viitattu 14.8.2015. (englanniksi)
- ↑ a b Jeremy M. Berg, John L. Tymoczko & Lubert Stryer: Biochemistry, 6th Edition, s. 702. W. H. Freeman and Company, 2006. ISBN 978-0-7167-8724-2. (englanniksi)
- ↑ a b c d e Clark A. Briggs, Mark W. Holladay, James F. Kerwin Jr., James P. Sullivan & Michael Williams: Neuroregulators, Kirk-Othmer Encyclopedia of Chemical Technology, John Wiley & Sons, New York, 2009. Viitattu 14.8.2015
- ↑ a b c Richard A Harvey,Denise R Ferrier: Lippincott's Illustrated Reviews: Biochemistry, s. 151. Lippincott Williams & Wilkins, 2010. ISBN 978-1-60831-412-6. Kirja Googlen teoshaussa (viitattu 14.8.2015). (englanniksi)
- ↑ a b c Eero Pesonen: Typpioksidin merkitys verenkierron patofysiologiassa. FINNANEST, 2006, 39. vsk, nro 2, s. 124–126. Artikkelin verkkoversio. Viitattu 25.10.2023.
- ↑ Elizabeth Martin,Robert Hine: A Dictionary of Biology, s. 307–308. Oxford University Press, 2015. ISBN 978-0-19-871437-8. Kirja Googlen teoshaussa (viitattu 14.8.2015). (englanniksi)
- ↑ a b Linda J. Van Eldik,D. Martin Watterson: Calmodulin and Signal Transduction, s. 288. Academic Press, 1998. ISBN 9780127138602. Kirja Googlen teoshaussa (viitattu 14.8.2015). (englanniksi)
- ↑ a b Perry A. Frey, Robert H. Ables & Adrian D. Hegeman: Enzymatic reaction mechanisms, s. 738–739. Oxford University Press, 2007. ISBN 978-0195122589. Kirja Googlen teoshaussa (viitattu 14.8.2015). (englanniksi)
