Vasta-aine

Vasta-aine eli immunoglobuliini (lyhenne Ig) tai antibodi[1] on nimi joukolle immuunijärjestelmän plasmasoluissa, B-soluissa ja muisti-B-soluissa olevia vesiliukoisia proteiineja. Plasmasolut erittävät vasta-aineita muun muassa vereen, imunesteeseen,[2] sylkeen, kyynelnesteeseen ja maitoon.[3] Vain leualliset selkärankaiset tuottavat vasta-aineita. Ihmisillä ja useimmilla muilla selkärankaisilla vasta-aineiden päätyyppejä eli isotyyppejä on 5. Nämä ovat IgA, IgD, IgE, IgG ja IgM.[4] Ihmisillä IgG:t jakautuvat alatyyppeihin IgG1, IgG2, IgG3 ja IgG4. IgA:t jakautuvat alatyyppeihin IgA1 ja IgA2. Ihmisillä IgG1:t ovat immuunipuolustuksen kannalta keskeisimpiä ja yleisimpiä veren vasta-aineista.[5]
Vasta-aineita käytetään monien sairauksien niin sanottuna biologisena hoitona[6].
Kunkin vasta-aineen toiminto on sitoutua vain tietynlaiseen virukseen, bakteeriin tai johonkin muuhun vasta-aineita tuottaneelle eliölle tuntemattomaan taudinaiheuttajaan, myrkkyyn tai muuhun haittatekijään. Sitoutuminen ei ole kovalenttista. Sitoutuminen voi estää haittatekijän toiminnan. Sitoutuminen voi tämän sijaan tai lisäksi myös merkitä haittatekijän tuhottavaksi.[2] Esimerkiksi makrofagit tunnistavat tiettyjä vasta-aineita ja tuhoavat niiden sitomia haittatekijöitä ottamalla niitä sisäänsä. Koska vasta-aineita on kehon nesteissä, niiden sanotaan olevan osa humoraalista immuunijärjestelmää (neste on latinaksi humor).[3]
Vasta-aineiden sitoutuminen voi myös olla haitallista. Ne voivat sitoutua vaarattomiin kehonulkoisiin aineisiin aiheuttaen allergioita tai vasta-aineita tuottaneen eliön omiin rakenneosiin aiheuttaen autoimmuunisairauksia. Vasta-aineet aiheuttavat myös hyljintäreaktioita elinsiirroissa ja keskenään epäsopivien verenluovuttajien välillä. Vasta-aineita käytetään myös lääketieteellisissä testeissä ja hoidoissa yleensä monoklonaalisten vasta-aineiden muodossa.[2]
Yksinkertaisimpien vasta-aineiden Y-kirjaimen muotoisen rakenteen kärjissä on kaksi identtistä aluetta, jotka sitoutuvat taudinaiheuttajaan tai johonkin muuhun aineeseen. Monimutkaisemmissa vasta-aineissa alueita tosin on enemmän. Näitä sitoutuvia alueita kutsutaan nimellä paratooppi. Paratoopin sitomaa ainetta, kuten taudinaiheuttajaa, sanotaan kokonaisuudessaan nimellä antigeeni.[3] Yksittäistä antigeenin kohtaa, johon paratooppi sitoutuu, kutsutaan nimellä epitooppi tai antigeeninen determinantti.[5]
Rakenne ja luokittelu[muokkaa | muokkaa wikitekstiä]
Perusrakenne[muokkaa | muokkaa wikitekstiä]

1. Fab-alueet
2. Fc-alue
3. raskasketju (siniset, vaaleasävyisimmät ovat vaihtelevia domeeneita)
4. kevytketju (vihreät, vaaleasävyisimmät ovat vaihtelevia domeeneita)
5. paratooppi eli antigeenin epitoopin sitova alue
6. sarana-alueet
-S-S-: disulfisidoksia. NH2: N-terminaali. COOH: C-terminaali.
Ihmisillä ja useilla muilla selkärankaisilla vasta-aineiden päätyyppejä on 5: IgA, IgD, IgE, IgG ja IgM.[3] Osa näistä on jaettavissa vielä useaan alatyyppiin.[5] Näistä IgD, IgE ja IgG koostuvat neljästä proteiinista: kahdesta yleensä identtisestä kevyt- eli L-ketjusta (eng. light) ja kahdesta yleensä identtisestä raskas- eli H-ketjusta (eng. heavy). Ketjut eivät ole täysin identtisiä eri vasta-ainetyyppien välillä. Raskasketjuissa on ne kahtia jakava taipunut "sarana-alue" (kuva, numero 6). Kevyt- ja raskasketjut ovat kiinni toisissaan disulfidisidoksin Y-kirjaimen muotoisena rakenteena.[3]

IgA ja IgM ovat samantapaisia kuin edellä kuvatut vasta-aineet, mutta IgA:t esiintyvät joko yksittäisinä Y:n muotoisina proteiineina (monomeereinä), kahden Y:n pareina (dimeereinä), kolmen Y:n rakenteina (trimeereinä)[3] tai neljän Y:n rakenteina (tetrameereinä).[5] IgM:t ovat kiinni solukalvoissa yksittäisinä monomereinä, solujen erittäminä viiden Y:n rakenteina (pentameereinä)[3] tai harvoin kuuden Y:n rakenteina (heksameereinä).[5]
Vasta-aineet ovat glykoproteiineja. Ne siis sisältävät erilaisia hiilihydraatteja, joiden sijainti vasta-aineen rakenteessa riippuu vasta-ainetyypistä. Vasta-ainetyypistä riippuen hiilihydraatit voivat estää vasta-aineiden hajoamista vakauttamalla niiden rakennetta tai olla välttämättömiä sille, että Fc-reseptorit sitoutuvat vasta-aineiden Fc-alueeseen.[5]
Kevyt- ja raskasketjut[muokkaa | muokkaa wikitekstiä]
Vasta-aineiden luokittelu päätyyppeihin perustuu vain niiden raskasketjuihin. Ihmisten vasta-aineissa kevytketjut ovat joko κ- tai λ-ketjuja. κ-ketjut ovat ihmisveren kaikista vasta-aineissa noin 1.5–2-kertaa yleisempiä kuin λ-ketjut, mutta suhdeluku vaihtele vasta-aineesta riippuen. IgA:issa esimerkiksi pääosa on λ-ketjuja.[7]
Ihmisillä raskasketjutyyppejä on 5 ja vasta-aineen[3]
- IgA raskasketjut ovat α-ketjuja
- IgD raskasketjut ovat δ-ketjuja
- IgE raskasketjut ovat ε-ketjuja
- IgG raskasketjut ovat γ-ketjuja
- IgM raskasketjut ovat μ-ketjuja
Kevyt- ja raskasketjuissa on vakiorakenteisia osia ja rakenteeltaan vaihtelevia osia. Nämä osat ovat proteiinidomeeneita. Vakiodomeenit eivät sitoudu antigeeneihin ja niiden rakenne on nimensä mukaisesti muuttumaton: ne ovat samanlaisia esimerkiksi kaikissa κ-ketjuissa. Vaihtelevat domeenit sisältävät antigeeniin sitoutuvan alueen ja siksi pelkästään vaihtelevan domeenin rakenne määrittää mihin antigeeniin vasta-aine sitoutuu. Vaihtelevat domeenit voivat olla erilaisia esimerkiksi eri vasta-aineiden κ-ketjuissa. Vakiodomeenien lukumäärä riippuu vasta-ainetyypistä (taulukko alla).[5]
| Ketju | Tyyppi | Vasta-aine, jonka osa ketju on | Vaihtelevien domeenien lukumäärä | Vakiodomeenien lukumäärä |
|---|---|---|---|---|
| κ | kevyt | IgA, IgD, IgE, IgG tai IgM | 1 | 1 |
| λ | kevyt | IgA, IgD, IgE, IgG tai IgM | 1 | 1 |
| α | raskas | IgA | 1 | 3 |
| δ | raskas | IgD | 1 | 3 |
| ε | raskas | IgE | 1 | 4 |
| γ | raskas | IgG | 1 | 3 |
| μ | raskas | IgM | 1 | 4 |
Fab- ja Fc-alue[muokkaa | muokkaa wikitekstiä]
Kunkin vasta-aineen Y:n muotoisessa rakenteessa on kaksi Fab-aluetta ja yksi Fc-alue. Raskasketjujen sarana-alue erottaa alueet nimellisesti. Muun muassa IgG:ssä alueet voidaan varsinaisesti irrottaa toisistaan käsiteltäessä IgG esimerkiksi papaiinientsyymillä.[3]
Fab tulee englanninkielen sanoista fragment-antigen-binding, "osa-antigeeni-sitova", sillä nämä osat sisältävät antigeeniä sitovat alueet. Fab-alueet sisältävät antigeeniä sitovat alueet ja ne koostuvat osin kevyt- ja raskasketjuista. Fc tulee sanoista fragment-crystallize, "osa-kiteytyä", sillä tämä osa kiteytyy helposti muiden Fc-alueiden kanssa, jos Fc-alueet on irrotettu Fab-alueista. Fc-alueet koostuvat pelkästään raskasketjuista. Fc-alueet sitoutuvat erilaisiin Fc-reseptoreihin, joita on muun muassa tiettyjen immuunijärjestelmän solujen, kuten makrofagien, pinnoilla.[3]
Ihmisten vasta-aineet[muokkaa | muokkaa wikitekstiä]
Ihmisten vasta-aineiden päätyypit ovat A, D, E, G ja M. Immunoglobuliini A:ta esiintyy etenkin hengitysteiden ja suolen limakalvoilla, joissa ne suojaavat yksilöä hengitystie- ja vatsasuolikanavan infektiolta[8].
Immunoglobuliini A jaetaan kahteen alatyyppiin, jotka ovat IgA1 ja IgA2. Veressä IgA:ista yli 90 % on IgA1:iä loppujen ollessa IgA2:ia. IgA2:t taas ovat yleisempiä limakalvojen eritteissä. IgA1:ssä raskasketjun sarana-alue on pidempi ja siksi tietyt bakteerien proteaasit pystyvät katkaisemaan sen helpommin kuin IgA2:ssa. IgG:t taas jaetaan neljään alatyyppiin, jotka ovat IgG1, IgG2, IgG3 ja IgG4. Veressä yleisin on IgG1. Pienten rakenne-erojen takia nämä alatyypit sitoutuvat parhaiten eri antigeeneihin.[5]
IgG2 ja IgG4 ovat jaettavissa sarana-alueensa disulfidisidosten puolesta edelleen eri alatyyppeihin. IgG2:n alatyyppejä on 3: IgG2-A/A, IgG2-B/B ja IgG2-A/B. IgG2-A/A:ssa sarana-alueella raskasketjujen välillä disulfidisidoksia on 4, IgG2-B/B:ssä niitä on 2 ja IgG2-A/B:ssä niitä on 3.[5]
IgG4:stä on 2 alatyyppiä, joista ensimmäinen on sitoo yhdenlaisia epitooppeja. Se on siis "monospesifinen", kuten vasta-aineet yleensä. Toinen tyyppi taas sitoo poikkeuksellisesti kahdenlaisia epitooppeja, eli se on "bispesifinen". Kuten muutkin ihmisten vasta-aineet, IgGA:t koostuvat kahdesta puolikkaasta. Puolikkaista kummassakin on yksi raskas- ja yksi kevytketju. Puolikkaat ovat kiinni sarana-alueelta kahdella disulfidisidoksella, mutta sidokset voivat välillä katketa ja muodostua uudelleen eräänlaisessa kehossa vallitsevassa tasapainoreaktiossa. Sidosten katketessa puolikkaat voivat irrota toisistaan täysin ja vaihtua toisen puolikkailtaan irtonaisen IgG4:n kanssa. Tällöin muodostuu bispesifinen IgG4.[5]
| Tyyppi | Kvaternääninen rakenne[5] | Kuvaus | Fc-reseptori, joka voi sitoa vasta-aineen[5] |
|---|---|---|---|
| IgA1 | monomeeri, dimeeri ja joskus trimeeri tai tetrameeri | Suojaa limakalvoja taudinaiheuttajilta. IgA1 on tosin harvinaisempi limakalvoilla kuin IgA2. IgA1 on IgA2:ta yleisempi veressä.[5] | CD89 (FCAR)[5] |
| IgA2 | monomeeri, dimeeri ja joskus trimeeri tai tetrameeri | Suojaa limakalvoja taudinaiheuttajilta. Yleinen limakalvoilla ja eritteissä, kuten syljessä ja maidossa. IgA2 on paljon yleisempi limakalvoilla kuin IgA1.[5] | CD89 (FCAR)[5] |
| IgD | monomeeri | Muodostuu IgM:n ohella luuytimessä vastamuodostuneissa B-soluissa ennen B-solujen läpikäymää luokanvaihtoa. IgD:n biologinen merkitys tunnetaan huonosti.[9] | FcδR[5] |
| IgE | monomeeri | Suojaa eritoten loisina eläviltä madoilta. Osallistuu usein allergisten reaktioiden syntyyn näitä reaktioita estivällä tavalla.[5] | FCER1 tai II (CD32)[5] |
| IgG1 | monomeeri | Yleinen veressä. Läpäisee istukan tehokkaasti ja voi siirtyä sikiöön. Sitoutuu lähinnä proteiineihin. Aktivoi komplementtijärjestelmän C1q-välitteisesti, muttei yhtä tehokkaasti kuin IgG3.[10] | I (CD64), II (CD32) tai III (CD16)[5] |
| IgG2 | monomeeri | Yleinen veressä. Läpäisee istukan ja voi siirtyä sikiöön, mutta huonommin kuin muut IgG:t. Sitoutuu eritoten hiilihydraatteihin. Muodostaa pääasiallisen vasta-ainevälitteisen suojan sellaisia bakteereita vastaan, joilla on hiilihydraatteja pinnallaan.[10] | II (CD32)[5] |
| IgG3 | monomeeri | Yleinen veressä. Läpäisee istukan tehokkaasti ja voi siirtyä sikiöön. Sitoutuu lähinnä proteiineihin ja suojaa eritoten viruksilta. Aktivoi tehokkaasti komplementtijärjestelmän C1q-välitteisesti. Järjestelmä edistää muun muassa kalvotuhokompleksin muodostumista taudinaiheuttajan solukalvoon.[10] | I (CD64), II (CD32) tai III (CD16)[5] |
| IgG4 | monomeeri | Yleinen veressä. Läpäisee istukan ja voi siirtyä sikiöön. Sitoutuu lähinnä proteiineihin. IgG4-vasta-aineita muodostuu pitkäaikaisessa altistuksessa tartuntatauteihin liittymättömille antigeeneille. Näin voi käydä esimerkiksi immunoterapiassa, jonka aineille henkilö on allerginen.[10] | I (CD64), II (CD32)[5] |
| IgM | monomeeri, pentameeri tai harvoin heksameeri | Muodostuu IgD:n ohella luuytimessä vastamuodostuneissa B-soluissa ennen solujen läpikäymää luokanvaihtoa.[11] IgM toimii varhaisessa vasta-ainevälitteisessä immuunipuolustuksessa ennen kuin muita vasta-aineita ehtii muodostumaan.[5] | FcμR[12] |
Muiden eliöiden vasta-aineet[muokkaa | muokkaa wikitekstiä]
Eliöistä vain leualliset selkärankaiset tuottavat vasta-aineita. Esimerkiksi leuattomat kalat käyttävät variaabeleja lymfosyyttireseptoreita mukautuvaan immuunipuolustukseensa vasta-aineiden sijaan. Vasta-ainetyypit vaihtelevat eliöiden välillä, joten myös tyypin määrittävät raskasketjut vaihtelevat. Vasta-aineiden päätyypit ovat yleensä[4]
- nisäkkäillä IgA, IgD, IgE, IgG ja IgM
- linnuilla IgA, IgM ja IgY (tämän raskasketju on ν)
- matelijoilla IgA, IgD, IgM, IgY ja joillakin myös IgD2 (tämän raskasketju on δ2)
- sammakkoeläimillä IgD, IgM, IgX (tämän raskasketju on χ) ja joillakin myös IgF (tämän raskasketju on ϕ)
- luukaloilla IgD, IgM ja joillakin yös IgT (tämän raskasketju on τ)
- rustokaloilla IgM, IgW (tämän raskasketju on ω) ja joillakin myös IgNAR (tämän raskasketju on NAR)
Myös kevytketjut vaihtelevat. Nisäkkäillä ja matelijoilla kevytketjuja on yleensä 2: κ- ja λ-ketjut. Luukaloilla ja sammakkoeläimillä kevytketjuja on 3: κ-, λ- ja σ-ketjut. Linnuilla on vain κ-kevytketjuja. Kamelieläimillä on vasta-aineita, joissa ei ole lainkaan kevytketjuja.[7]
Biologinen toiminta[muokkaa | muokkaa wikitekstiä]
Vasta-aineet sitoutuvat niitä tuottaneelle eliölle haitallisiin tekijöihin ei-kovalenttisesti.[2] Sidos on silti usein hyvin vahva ja sen dissosiaatiovakio on kertaluokkaa 1·10–8–1·10–12.[13] Haittatekijät voivat olla esimerkiksi virusten tartuttamia soluja, viruksia, bakteereita, myrkyllisiä proteiineja (esimerkiksi bakteerien tuottamia) tai alkueläimiä.[2] Vasta-aineiden sitomien aineiden massa ei yleensä ole alle 5 000 g/mol, mutta pienetkin molekyylit voivat aiheuttaa vasta-ainevälitteisen immuunireaktion sitoutumalla isompiin aineisiin hapteeneina, jolloin ison aineen rakenne muuttuu siten että siihen muodostuu jokin antigeeninen alue eli epitooppi ja jokin vasta-aine voi sitoutua siihen.[3]

Vasta-aine voi sitoutumalla haittatekijään neutraloida sen, jolloin tekijä ei saa aikaan haitallisia vaikutuksiaan. Esimerkiksi viruksessa vasta-aine voi sitoutua johonkin sen tartunnan kannalta välttämättömistä pintaproteiineista, jolloin virus ei pysty tartuttamaan soluja.[2]
Vasta-aine voi neutralisoinnin lisäksi tai sen sijaan sitoutumisellaan merkitä haittatekijän makrofagien tuhottavaksi. Koko tapahtumaa sanotaan opsonisaatioksi. Vasta-aine voi liittyä esimerkiksi bakteeriin. Makrofagi tunnistaa sitoutuneen vasta-aineen ja tuhoaa bakteerin nielemällä sen. Tapahtuu siis fagosytoosi.[2] Tunnistus tapahtuu makrofagin pinnassa olevien Fc-reseptorien avulla, jotka sitoutuvat vasta-aineen Fc-alueeseen (katso kohta Fab- ja Fc-alue).[3] Muun muassa ihmisillä Fc-reseptoreita on useita erilaisia, joista kukin sitoutuu vain tietyntyyppisiin vasta-aineisiin. Fc-reseptoreita on muissakin soluissa.[5] Koska kussakin vasta-aineessa on vähintään kaksi antigeeniä sitovaa kohtaa, ne voivat liittää useita haittatekijöitä yhteen estäen niiden leviämistä. Tätä sanotaan aggregaatioksi tai agglutinaatioksi. Makrofagit voivat tuhota kertymän.[2]
Vasta-aineen sitoutuminen haittatekijään voi myös aktivoida komplementtijärjestelmän. Tämä saa aikaan kalvotuhokompleksin (eng. membrane attack complex, MAC) muodostumisen haittatekijän solukalvoon. Yleensä tekijä on bakteeri. MAC muodostaa reiän kalvoon, jolloin ioneita ja vettä virtaa hallitsemattomasti bakteerin sisään, bakteeri turpoaa ja lopulta halkeaa. Komplementtijärjestelmän aktivaatio myös lisää paikallisesti tulehdusta ja fagosytoosia, jotka edistävät haittatekijöiden tuhoamista.[2]
Geenit[muokkaa | muokkaa wikitekstiä]
Ihmisillä vasta-aineiden raskasketjuja koodaa geeni IGH. Se on kromosomissa 14 kohdassa 14q32.33. Sen pituus on yleensä noin 1 250 kiloemäsparia (kb). Kappa-(κ-)kevytketjua koodaa geeni IGK. Se on kromosomissa 2 kohdassa 2p11.2. Sen pituus on yleensä noin 1 820 kb. Lambda-(λ-)kevytketjua koodaa geeni IGL. Se on kromosomissa 22 kohdassa 22q11.2. Sen pituus on yleensä noin 1 050 kb. Edeltävissä geeneissä on eri alueita, joita ovat[14]
- V-alueet (eng. variable) eli vaihtelevat alueet
- D-alueet (eng. diversity) eli monimuotoisuusalueet
- J-alueet (eng. joining) eli liitosalueet
- C-alueet (eng. constant) eli vakioalueet
Nämä geenien alueet koodaavat samannimisiä proteiinidomeeneita vasta-aineproteiineissa. D-alueita on vain raskasketjujen IGH-geenissä. Tässä geenissä D-, J- ja C-alueita on vastaavasti 23, 6 ja 9. IGK-geenissä J- ja C-alueita on vastaavasti 5 ja 1. IGL-geenissä J- ja C-alueita on vastaavasti 4–5 ja 4–5. V-alueiden määrä IGH-, IGK- ja IGL-geeneissä vaihtelee riippuen ihmisestä. Kussakin geenissä on noin 30–50 V-aluetta.[14]
Muodostuminen[muokkaa | muokkaa wikitekstiä]
Eliöt pystyvät tuottamaan vain muutaman vasta-ainetyypin. Näistä kussakin on kuitenkin rakenteeltaan vaihtelevia alueita, joiden rakennevaihtelun takia esimerkiksi ihmiset voivat teoriassa tuottaa ainakin sata miljardia (1011) eri vasta-ainetta. Näistä kukin voi vaihtelevista alueistaan sitoutua ainakin yhteen keskenään erilaiseen epitooppiin antigeeneissä. Vasta-ainevaihtoehtojen lukumäärän takia eliöt voivat periaatteessa tuottaa vasta-aineen mitä tahansa taudinaiheuttajaa tai muuta eliölle haitallista tekijää vastaan. Ihmisillä vastamuodostuneet B-solut läpikäyvät luuytimessä V(D)J-rekombinaation, joka saa aikaan osan miljardeista vasta-ainevaihtoehdoista. Rekombinaatiossa karsitaan vasta-ainegeenien V-, D- ja J-alueita, joita on monia (katso kohta geenit).[14]
Sitten vasta-aineista tehdään itsetolerantteja: tässä vaiheessa B-soluista karsitaan pois ne, jotka tuottavat kehon omiin osiin sitoutuvia ja siksi haitallisia vasta-aineita. Karsinta tapahtuu ensin luuytimessä, josta solut sitten vapautuvat. Loppukarsinta tapahtuu pääosin imusuonistossa.[14]
Kohdatessaan antigeenin, B-solut läpikäyvät luokanvaihdon, jossa aiemmin vain IgD- ja IgM-vasta-aineita tuottava solu erikoistuu tuottamaan vain IgA-, IgE- tai IgG-vasta-aineita. Luokanvaihdossa karsitaan vasta-ainegeenien C-alueita.[14] Ihmisillä pieni määrä poikkeuksellisia B-soluja voi tosin erikoistua tuottamaan vain IgD:itä.[9]
Antigeenin kohtaamisen seurauksena B-solu myös jakautuu useasti imusuoniston itukeskuksissa. Kussakin jakautumisessa tapahtuu tarkoituksenmukaisia mutaatioita vasta-aineiden geeneissä, jotka lisäävät vasta-ainekirjoa V(D)J-rekombinaation tapaan. Näitä mutaatioita kutsutaan nimellä somaattinen hypermutaatio.[5]
V(D)J-rekombinaatio[muokkaa | muokkaa wikitekstiä]
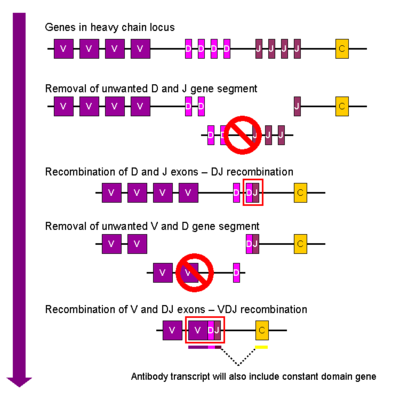
1. muuntumaton raskasketjun geeni
2. osa D- ja J-alueista poistuu satunnaisesti RAG1-2:n avulla
3. DJ-alue muodostuu
4. osa V- ja J-alueista poistuu satunnaisesti RAG1-2:n avulla
5. VDJ-alue muodostuu
Muun muassa ihmisillä vastamuodostuneen B-solun kehittyessä luuytimessä, RAG1-2-entsyymi katkaisee satunnaisesti kaksi kohtaa solun raskasketjua koodaavan DNA:n D- ja J-alueiden vierestä. Katkaistujen kohtien välinen alue DNA:sta leikkautuu pois ja muut entsyymit liittävät D- ja J-alueet yhteen DJ-alueeksi eli eheäksi DNA-ketjuksi. D- ja J-alueita on monia, joten ne voivat tuottaa useita eri DJ-yhdistelmiä. Sitten DJ-alue liittyy samalla tavoin RAG1-2-välitteisesti ja satunnaisesti johonkin kymmenistä V-alueista. Muodostuu VDJ-alue, joka on lopullinen osa B-solun DNA:ta. Koko tapahtumaa sanotaan V(D)J-rekombinaatioksi. Sama ylimääräistä DNA:ta karsiva ja sitä satunnaisesti eri tavoin yhdistelevä rekombinaatio tapahtuu myös kevytkejuille, mutta niissä ei ole D-alueita, jota nimen "V(D)J" sulut merkitsevät. Rekombinaation jälkeen B-solut voivat tuottaa silmukoitumisen kautta IgD- ja IgM-vasta-aineita.[14]
V-, D- ja J-alueita on kutakin useampi kuin yksi, joten osittain niiden mahdollisten yhdistelmien takia ihmiset voivat suuren määrän eri vasta-aineita.[14] Esimerkiksi ihmisten raskasketjun geenissä D-, J- ja V-alueita on vastaavasti 23, 6 ja noin 40 (katso kohta geenit). Näiden yhdistelmiä on 23×6×40 = 5 520. κ- ja λ-kevytketjun geeneissä J- ja V-alueita on kummassakin vastaavasti 5 ja noin 40, joten yhdistelmiä on 200. Ihmisillä V(D)J-rekombinaatio tuottaa siten 5 520×200×200 ≈ 220 miljoonaa erilaista vasta-ainetta. Luokanvaihto ja somaattiset hypermutaatiot lisäävät määrää entisestään.
Itsetoleranssi[muokkaa | muokkaa wikitekstiä]
V(D)J-rekombinaatiossa sattuu virheitä eli mutaatioita. Siksi siinä muodostuu jonkin verran B-soluja, jotka eivät pysty tuottamaan vasta-aineita. V(D)J-rekombinaatio on myös satunnaista, jonka takia ihmisillä jopa 50–80 % siinä tuotetuista vasta-aineista sitoutuu kehon omiin aineisiin. Nämä voisivat aiheuttaa immuunijärjestelmän hyökkäyksen eliötä itseään vastaan. Tällaisia vasta-aineita tuottavat B-solut kuitenkin karsitaan pääosin pois luuytimessä ja pienempi osa karsitaan myöhemmin imusuonistossa monimutkaisin mekanismein. Tällöin vasta-aineet kehittyvät sietämään eliötä itseään, eli vasta-aineet ovat itsetolerantteja. Mekanismit voivat tosin poikkeustiloissa toimia virheellisesti. Tämä voi johtaa erilaisiin autoimmuunisairauksiin, joissa vasta-aineet hyökkäävät eliötä itseään vastaan, tai perinnöllisiin immuunikatosairauksiin, joissa toimivia vasta-aineita ei muodostu tarpeeksi.[15]
Luuytimessä tapahtuvia itsetoleranssia kehittävien suojamekanismien kokonaisuutta sanotaan englanniksi nimellä central tolerance eli keskustoleranssi. Mekanismi on epätäydellinen ja ihmisillä tämän käsittelyn jälkeen noin 10 % luuytimestä vapautuneista B-soluista ei ole tuottamiltaan vasta-aineiltaan itsetolerantteja. Muualla kuin luuytimessä tapahtuvat mekanismit poistavat pääosan lopuista ei-itsetoleranteista vasta-aineista. Näitä myöhempiä mekanismeja sanotaan nimellä peripheral tolerance eli ääreistoleranssi.[15]
Ihmisillä V(D)J-rekombinaation läpikäyneet, mutta vielä epäkypsät ja luuytimessä olevat B-solut tuottavat pinnoilleen IgM:iä ja IgD:itä.[9] Nämä muodostavat B-solun pinnalla olevien CD79A-CD79B- eli Igα-Igβ-proteiiniparien kanssa B-solureseptoriksi (BCR) kutsutun kokonaisuuden. Reseptorin osana oleva vasta-aine voi sitoa antigeenin, jotka ovat yleensä tässä vaiheessa kehon omia luuytimessä olevia aineita. BCR:n kautta välittyy vahva vaste jos vasta-aine sitoutuu johonkin kehon omaan aineeseen. Solun tuottamat vasta-aineet ovat tällöin todennäköisesti haitallisua ihmiselle eli ei-itsetolerantteja. Keskivahva vaste ilmenee, jos BCR ei sitoudu mihinkään antigeeniin. Vastetta ei ole, jos B-solun vasta-ainegeenit ovat virheellisen V(D)J-rekombinaation seurauksena toimimattomat.[15]
Epäkypsiä B-soluja siis testataan ennen kuin ne kypsyvät osaksi immuunijärjestelmää. Solu aistiin BCR:n vasteen. Vasteen aiheuttamattomat eli vasta-aineiltaan toimimattomat B-solut ja liian vahvan vasteen aiheuttavat haitalliset B-solut kuolevat apoptoosin kautta tai sitten ne läpikäyvät reseptorimuokkauksen (eng. receptor editing). Reseptorimuokkaus on näiden ongelmien pääasiallinen käsittelytapa. Siinä B-solu läpikäy V(D)J-rekombinaation uudelleen ja viallinen/haitallinen solu yritetään korjata tuhoamisen sijaan.[14]
Keskustoleranssijärjestelmän käsittelyn B-solut poistuvat luuytimestä. Kaikkia kehon mahdollisina antigeeneinä toimivia aineita ei ole luuytimessä ja osin tästä syystä B-solut läpikäyvät ääreistoleranssin käsittelyn. Tämä käsittely tapahtuu lähinnä haimassa ja imusuonistossa. Käsittelyssä on paljon palautuvia mekanismeja. Se on siten mukautuvampi kuin keskustoleranssin käsittely. Ääreistoleranssin tulee sallia sellaisten vasta-aineiden tuotto, jotka saattavat sitoutua paratoopeistaan jossain määrin myös kehon omiin osiin. Taudinaiheuttajissa voi nimittäin olla epitooppisia rakenteita, jotka ovat samankaltaisia kuin jotkin ihmiskehon aineissa.[15]
Luokanvaihto[muokkaa | muokkaa wikitekstiä]

1. V(D)J-rekombinaation läpikäynyt raskasketjun geeni.
2. C-alueet leikkautuvat pois S-alueiden kohdalta.
3. Jäljelle jäävän geenin ja pois leikkautuneen alueen S-alueet liittyvät yhteen.
Normaalisti luokanvaihto eli isotyypin vaihto tapahtuu B-solun pinnan IgM:n tai IgD:n sitoessa keholle vieras antigeeni. Luokanvaihdossa V(D)J-rekombinaation läpikäyneistä B-soluista kukin erikoistuu tuottamaan joko IgA-, IgE tai IgG-vasta-aineita. Ennen luokanvaihtoa nämä B-solut voivat tuottaa vain IgD- ja IgM-vasta-aineita.[14] Ihmisillä on tosin pieni määrä poikkeuksellisia soluja nielun imukudoksessa (muun muassa nielurisoissa), jotka erikoistuvat tuottamaan vain IgD:itä.[9] Luokanvaihto on myös rekombinaatioreaktio ja se tapahtuu luuytimessä. Toisin kuin V(D)J-rekombinaatio, luokanvaihto ei ole satunnainen tapahtuma vaan säädelty.[11]
Luokanvaihdossa B-solun DNA:sta poistetaan ylimääräiset C-alueet katkaisemalla DNA kahdesta kohtaa C-alueita sisältävältä alueelta. Katkeamiskohtien väliin jäävä alue poistuu ja liittyy päistään itsensä sulkevaksi silmukaksi. Katkeaminen tapahtuu S-alueiden kohdalta. S-kirjain tulee englanninkielen sanasta switch. S-alueet ovat C-alueiden vieressä DNA:n 5'-pään puolella. Aktivaation indusoima sytidiinideaminaasi -entsyymi aloittaa luokanvaihdon deaminoimalla S-alueiden sytosiineja urasiileiksi. Katkeaminen tapahtuu näiden urasiilien kohdalta DNA:n korjausmekanismin emäksen korjausentsyymien avulla. Katkenneet päät liitetään taas yhtäjaksoiseksi DNA:ksi perimän korjausmekanismein, jolloin luokanvaihto on valmis.[11]
Somaattinen hypermutaatio[muokkaa | muokkaa wikitekstiä]
Ihmisillä ja muilla eliöillä V(D)J-rekombinaation, luokanvaihdon ja itsetoleranssitestit läpikäyneen B-solun altistuessa imusuonistossa sen vasta-aineisiin sitoutuvalle antigeenille, solu alkaa jakautua nopeasti jossakin imusuoniston itukeskuksessa. Jakautumisessa B-solun DNA:ssa tapahtuu tarkoituksenmukaisesti tietynlaisia satunnaisia mutaatioita, jotka muuntavat kunkin jakautuneen solun vasta-aineiden sitoutumisherkkyyttä eri vasta-aineille. Tapahtumaa sanotaan somaattiseksi hypermutaatioksi ja se lisää vasta-ainekirjoa entisestään. Ihmisillä tapahtuman mutaatiotaajuus on suunnilleen 1 mutaatio per 1 000 DNA:n emästä per solujakautuminen.[5]
Käyttökohteet[muokkaa | muokkaa wikitekstiä]
Lääkekäyttö[muokkaa | muokkaa wikitekstiä]
Vasta-aineita käytetään lääkkeinä moniin sairauksiin. Joitakin esimerkkejä ovat syövät, geneettiset sairaudet ja autoimmuunisairaudet, kuten nivelreuma, psoriasis, colitis ulcerosa ja punahukka. Markkinoilla on suuri määrä vasta-ainelääkkeitä, joista muutamia esimerkkejä ovat adalimumabi, bevasitsumabi, Infliksimabi ja rituksimabi[16] sekä MS-tauti [6].
Immunoglobuliini G:tä (IVIG) käytetään esimeriksi dermatomyosiittiin, Guillain–Barre oireyhtymään, krooniseen tulehdukselliseen myeliiniä tuhoavaan polyneuropatiaan, multifokaaliseen mogtoriseen neuropatiaan ja myasthenia gravikseen sekä eräisiin ihosairauksiin[17].
Vasta-aineita käytetään myös kohdentamaan niihin liitettyjä aineita tiettyihin kudoksiin. Vasta-aineisiin voi esimerkiksi olla liitettynä radioaktiivisia isotooppeja, jotka vasta-aine kohdentaa syöpäkasvaimeen osana syöpähoitoa: tätä sanotaan radioimmunoterapiaksi.[18]
Lääkinnälliset vasta-aineet ovat usein kimeerisiä tai humanisoituja monoklonaalisia vasta-aineita, jotka on tuotettu muissa eläimissä kuin ihmisissä. Kimeerisissä vasta-ainelääkkeissä niiden nimen pääte on usein "-ksimabi" ja niissä jopa 65 % eläimen vasta-aineen rakenteesta on tehty geenimuuntelun avulla samanlaisiksi kuin ihmisillä. Humanisoiduissa vasta-ainelääkkeissä nimen pääte on usein "-tsumabi" ja niiden rakenteesta noin 95 % on tehty samanlaisiksi kuin ihmisillä. Muuntelun takia ihmiskehon immuunijärjestelmä ei tunnista näitä vasta-ainelääkkeitä yhtä herkästi vieraiksi aineiksi, kuin ilman muuntelua, ja ala hylkimään lääkkeitä, jolloin voisi ilmetä haittavaikutuksia.[18]
Aineiden havaitseminen[muokkaa | muokkaa wikitekstiä]
Vasta-aineita käytetään tieteellisessä tutkimuksessa erilaisten aineiden mittauksessa. Lääketieteessä niitä käytetään esimerkiksi joidenkin sairauksien, myrkytysten tai päihteiden käytön havaitsemiseen. Vasta-aineet voivat sitoutua vaikkapa verinäytteestä, virtsasta tai syljestä löytyviin hormoneihin (esimerkiksi raskaudesta kertova istukkahormoni), bakteereihin (esimerkiksi streptokokit, klamydia ja Helicobacter pylori), viruksiin (esimerkiksi B- ja C-hepatiitti), loisiin (esimerkiksi malaria), päihteisiin tai sairauksista kieliviin biomarkkereihin, kuten sydänlihasvauriossa ilmenevään troponiiniin tai eturauhassyövässä muodostuvaan prostataspesifiseen antigeeniin. Näiden aineiden havaitseminen tai viitearvoista poikkeava määrä voi auttaa lääketieteellisen diagnoosin tekemisessä.[19]
Vasta-aineita käyttävissä tutkimusmenetelmissä havaitseminen perustuu usein jonkin aineen väriin, fluoresenssiin tai luminesenssiin. Aine voi olla vasta-aine itse, joka sitoutumisellaan leimaa jonkin tietyn aineen, jolloin vasta-aineen sitova aine on havaittavissa eri menetelmin. Leima-aineina saatetaan harvoin käyttää myös radioaktiivisia isotooppeja (katso isotooppileimaus).[19]
Vasta-aineita käyttäviä tutkimusmenetelmiä on monia. Esimerkkejä ovat ELISA, Western blot, yksinkertaiset testitikut (esimerkiksi raskaustestit) ja fluoresenssipolarisaatioimmunomääritys (FPIA). Kudostutkimuksessa voidaan käyttää fluoresoivia aineita sisältäviä vasta-aineita, jotka kohdentuvat tiettyihin soluihin tai kohtiin kudoksissa. Nämä fluoresoivat aineet voidaan havaita valomikroskoopilla, fluorometrillä tai virtaussytometrillä.[19]
Katso myös[muokkaa | muokkaa wikitekstiä]
Lähteet[muokkaa | muokkaa wikitekstiä]
- DL Nelson et al: Lehninger principles of biochemistry. 5. painos. W.H. Freeman, 2008. ISBN 9780716771081.
Viitteet[muokkaa | muokkaa wikitekstiä]
- ↑ Eläintiede:vasta-aine – Tieteen termipankki tieteentermipankki.fi. Viitattu 1.4.2020.
- ↑ a b c d e f g h i LA Urry et al: Campbell biology, s. 960–972. 11. painos. Pearson, 2017. ISBN 9780134093413.
- ↑ a b c d e f g h i j k l Nelson, s. 170–175
- ↑ a b R Pettinello, H Dooley: The immunoglobulins of cold-blooded vertebrates. Biomolecules, 2014, 4. vsk, nro 4, s. 1045–1069. PubMed:25427250. doi:10.3390/biom4041045. ISSN 2218-273X. Artikkelin verkkoversio.
- ↑ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab HW Schroeder, L Cavacini: Structure and function of immunoglobulins. The Journal of allergy and clinical immunology, 2010, 125. vsk, nro 202, s. S41–S52. PubMed:20176268. doi:10.1016/j.jaci.2009.09.046. ISSN 0091-6749. Artikkelin verkkoversio.
- ↑ a b Immunoglobuliinin käyttö neurologisten tautien hoidossa www.duodecimlehti.fi. Viitattu 30.4.2023.
- ↑ a b CL Townsend et al: Significant differences in physicochemical properties of human immunoglobulin kappa and lambda CDR3 regions. Frontiers in Immunology, 2016, 7. vsk. PubMed:27729912. doi:10.3389/fimmu.2016.00388. ISSN 1664-3224. Artikkelin verkkoversio.
- ↑ S -Immunoglobuliini A LOUNA Lab. Viitattu 3.1.2024.
- ↑ a b c d C Gutzeit, K Chen, A Cerutti: The enigmatic function of IgD: some answers at last. European journal of immunology, 2018, 48. vsk, nro 7, s. 1101–1113. PubMed:29733429. doi:10.1002/eji.201646547. ISSN 0014-2980. Artikkelin verkkoversio.
- ↑ a b c d G Vidarsson, G Dekkers, T Rispens: IgG subclasses and allotypes: from structure to effector functions. Frontiers in Immunology, 20.10.2014, 5. vsk. PubMed:25368619. doi:10.3389/fimmu.2014.00520. ISSN 1664-3224. Artikkelin verkkoversio.
- ↑ a b c J Stavnezer, CE Schrader: Ig heavy chain class switch recombination: mechanism and regulation. Journal of immunology, 2014, 193. vsk, nro 11, s. 5370–5378. PubMed:25411432. doi:10.4049/jimmunol.1401849. ISSN 0022-1767. Artikkelin verkkoversio.
- ↑ J Liu et al: Role of the IgM Fc receptor in immunity and tolerance. Frontiers in Immunology, 2019, 10. vsk. PubMed:30967868. doi:10.3389/fimmu.2019.00529. ISSN 1664-3224. Artikkelin verkkoversio.
- ↑ Nelson, s. 157
- ↑ a b c d e f g h i T Böldicke et al: Antibody Engineering. InTech, 2018. ISBN 9789535139751. Teoksen verkkoversio (viitattu 2.4.2020).
- ↑ a b c d D Nemazee: Mechanisms of central tolerance for B cells. Nature reviews. Immunology, 2017, 17. vsk, nro 5, s. 281–294. PubMed:28368006. doi:10.1038/nri.2017.19. ISSN 1474-1733. Artikkelin verkkoversio.
- ↑ A Saeed et al: Antibody engineering for pursuing a healthier future. Frontiers in Microbiology, 2017, 8. vsk. PubMed:28400756. doi:10.3389/fmicb.2017.00495. ISSN 1664-302X. Artikkelin verkkoversio.
- ↑ Clinical uses of intravenous immunoglobulin. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1809480/
- ↑ a b A Mahmuda et al: Monoclonal antibodies: a review of therapeutic applications and future prospects. Tropical Journal of Pharmaceutical Research, 2017, 16. vsk, nro 3, s. 713. doi:10.4314/tjpr.v16i3.29. ISSN 1596-9827. Artikkelin verkkoversio.
- ↑ a b c ME Koivunen, RL Krogsrud: Principles of immunochemical techniques used in clinical laboratories. Laboratory Medicine, 2006, 37. vsk, nro 8, s. 490–497. doi:10.1309/MV9RM1FDLWAUWQ3F. ISSN 0007-5027. Artikkelin verkkoversio.
Aiheesta muualla[muokkaa | muokkaa wikitekstiä]
 Kuvia tai muita tiedostoja aiheesta Vasta-aine Wikimedia Commonsissa
Kuvia tai muita tiedostoja aiheesta Vasta-aine Wikimedia Commonsissa