Formoteroli

| |
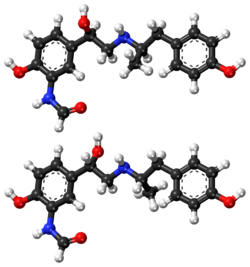
| |
Formoteroli
| |
| Systemaattinen (IUPAC) nimi | |
| N-[2-hydroksi-5-[1-hydroksi-2-[1-(4-metoksifenyyli)propan-2-yyliamino]etyyli]fenyyli]formamidi | |
| Tunnisteet | |
| CAS-numero | |
| ATC-koodi | R03 |
| PubChem CID | |
| DrugBank | |
| Kemialliset tiedot | |
| Kaava | C19H24N2O4 |
| Moolimassa | 344,402 |
| SMILES | Etsi tietokannasta: , |
| Fysikaaliset tiedot | |
| Sulamispiste | 138–140 °C (fumaraattisuolan dihydraattina)[1] |
| Farmakokineettiset tiedot | |
| Hyötyosuus | ? |
| Proteiinisitoutuminen | 61–64 %[2] |
| Metabolia | Hepaattinen |
| Puoliintumisaika | 10 h[2] |
| Ekskreetio | ? |
| Terapeuttiset näkökohdat | |
| Raskauskategoria |
? |
| Reseptiluokitus |
|
| Antotapa | Inhalaatio |
Formoteroli (C19H24N2O4) on aromaattinen orgaaninen yhdiste. Yhdistettä voidaan käyttää lääketieteessä keuhkoputkia laajentavana lääkeaineena astman ja keuhkoahtaumataudin hoidossa.[3]
Ominaisuudet ja käyttö[muokkaa | muokkaa wikitekstiä]
Formoterolia käytetään yleensä fumaraattisuolan dihydraattina, joka on kiteistä ainetta.[1] Lääkeaine vaikuttaa sitoutumalla β2-adenergisiin reseptoreihin ja on sen agonisti eli aktivoi sitä. Tämän seurauksena keuhkoputkia ympäröivä sileä lihaskudos rentoutuu ja keuhkoputket pääsevät laajenemaan. Formoterolin vaikutus alkaa noin 5 minuutin kuluttua lääkkeen oton jälkeen ja kestää noin 12 tuntia. Se kuuluu siis pitkävaikutteisiin β2-reseptorien agonisteihin. Formoteroli on kiraalinen yhdiste, jota myydään joko (R,R)- ja (S,S)-enantiomeerejä sisältävänä raseemisena seoksena tai pelkkänä (R,R)-enantiomeerina eli arformoterolina. (R,R)-enantiomeeri on lääkeaineena noin 1 000 kertaa (S,S)-enantiomeeria tehokkaampi. Formoterolia käytetään inhalaattoreissa erityisesti vaikean ja keskivaikean astman hoidossa yhdessä glukokortikoidien kanssa.[4][5][6][7][8]
Haittavaikutukset[muokkaa | muokkaa wikitekstiä]
Formoterolin aiheuttamia haittavaikutuksia voivat olla pääkipu, väsymys, nenän tukkoisuus, vatsakivut ja huonovointisuus.[7][8]
Valmistus[muokkaa | muokkaa wikitekstiä]
Formoterolin synteesin ensimmäisissä vaiheissa p-hydroksiasetofenoni nitrataan ja hydroksyyliryhmä suojataan bentsyylieetterinä. Seuraavassa vaiheessa suoritetaan bromaus ja tässä reaktiossa muodostuva tuote reagoi N-bentsyyli-1-(4-metoksifenyyli)propan-2-amiinin kanssa. Tämän jälkeen nitroryhmä pelkistetään raudan avulla aminoryhmäksi ja karbonyyliryhmä natriumboorihydridin avulla hydroksyyliryhmäksi. Seuraavaksi yhdiste reagoi muurahaishapon kanssa ja suojaryhminä toimivat bentsyyliryhmät poistetaan vedyttämällä. Näin muodostuu raseeminen seos. On myös kehitetty asymmetrinen synteesimenetelmä, jossa muodostuu ainoastaan formoterolin (R,R)-enantiomeeria.[5][8]
Lähteet[muokkaa | muokkaa wikitekstiä]
- ↑ a b Susan Budavari (päätoim.): Merck Index, s. 719. 12th Edition. Merck & Co., 1996. ISBN 0911910-12-3. (englanniksi)
- ↑ a b Formoterol DrugBank. Viitattu 19.8.2017. (englanniksi)
- ↑ Terveyskijrasto - Duodecim Terveyskirjasto. Viitattu 10.6.2019. [vanhentunut linkki]
- ↑ Hannu Kankaanranta & Eeva Moilanen: 30. Hengitysteiden sairauksien hoidossa käytettävät lääkeaineet Farmakologia ja toksikologia. Medicina. Viitattu 19.8.2017.
- ↑ a b Klaus J. Erb, Dominic H. Martyres & Peter Seither: Antiasthmatic Agents, Ullmann's Encyclopedia of Industrial Chemistry, John Wiley & Sons, New York, 2010. Viitattu 19.8.2017
- ↑ David A. Williams, William O. Foye, Thomas L. Lemke: Foye's principles of medicinal chemistry, s. 406. Lippincott Williams & Wilkins, 2012. ISBN 99781609133450. Kirja Googlen teoshaussa (viitattu 19.8.2017). (englanniksi)
- ↑ a b Jeffrey K. Aronson: Meyler's Side Effects of Drugs, s. 444. Elsevier, 2015. ISBN 9780444537171. Kirja Googlen teoshaussa (viitattu 19.8.2017). (englanniksi)
- ↑ a b c Ruben Vardanyan,Victor Hruby: Synthesis of Best-Seller Drugs, s. 362–363. Academic Press, 2016. ISBN 9780124114920. Kirja Googlen teoshaussa (viitattu 19.8.2017). (englanniksi)