Atomiteoria

Kemiassa ja fysiikassa atomiteoria on tieteellinen teoria, jonka mukaan kaikki aine koostuu diskreeteistä eli epäjatkuvista yksiköistä eli atomeista, jotka ovat kemiallisesti jakamattomia. Atomiteoriaa kuvataan atomimallien avulla. Atomiteorian avulla pystytään selittämään tiettyjä ilmiöitä, kuten miksi aineella on tietty olomuoto tietyssä lämpötilassa. Demokritos ja Demokritoksen oppi-isä Leukippos pohtivat aineen koostumusta ja päätyivät siihen, että aine koostuu atomeista, ja että atomi on jakamaton. Jakamaton on kreikaksi atomos, josta sana atomi on johdettu.[1] Nykyään atomien kuitenkin tiedetään koostuvan osasista ja atomeita voitavan jakaa fissioreaktioilla. Nykyisin on vallalla kvanttimekaaninen teoria, mutta sitä ovat edeltäneet Bohrin, Sommerfeldin, Rutherfordin ja Thomsonin teoriat.
Atomimallin kehitys[muokkaa | muokkaa wikitekstiä]
Varhaiset atomistit[muokkaa | muokkaa wikitekstiä]
- Pääartikkeli: Atomismi
Antiikin Kreikassa maailman ajateltiin koostuvan neljästä alkuaineesta, tulesta, vedestä, maasta ja ilmasta. Tämän ajattelumallin kehitti Empedokles 400-luvulla eaa. Myöhemmin Demokritos ja hänen opettajansa Leukipos kehittivät uuden mallin, jonka mukaan nämä neljä elementtiä koostuivat atomeista, jotka ovat jakamattomia ja niitä erottaa tyhjyys.[1] Antiikin tunnetuin filosofi Aristoteles ei kuitenkaan uskonut tyhjiön olemassaoloon ja näin kielsi Demokritoksen mallin.[2] Koska Aristoteleen kirjoitukset hallitsivat eurooppalaista sivistystä pitkälle keskiajalle saakka, jäi atomiteoria taka-alalle kahdeksi vuosituhanneksi.[1] Demokritoksen malli kuitenkin säilyi jälkipolville roomalaisen runoilijan Lucretiuksen teoksen De rerum natura (Maailmankaikkeudesta) ansiosta.[3][4]
Demokritoksen atomimalli on nykyiseen malliin verrattuna äärimmilleen yksinkertaistettu sekä virheellinen. Demokritoksen mallissa aine koostuu täysin jakamattomista atomeista. Nykymallissa todetaan kuitenkin että atomi jakaantuu kahteen osaan; ytimeen ja elektroniverhoon. Lisäksi Demokritos väitti eri aineiden atomien olevan erimuotoisia; veden atomien pyöreitä, tulen piikkisiä ja maa-atomien rosoisia. Oikeassa Demokritosta voidaan pitää siinä, että atomit ovat keskenään eri kokoisia, eri massaisia sekä osaltaan siinä että atomit ovat ikuisia.
Atomiteorian ensimmäiset tieteelliset todisteet[muokkaa | muokkaa wikitekstiä]
Robert Boyle (1627–1692) oli ensimmäisiä, jotka uudella ajalla herättivät atomihypoteesin henkiin. Hänen mukaansa kaikki aine koostui samanlaisista perushiukkasista eli korpuskelista, jotka eri aineissa olivat ryhmittyneet eri tavoilla.[5] Samoihin aikoihin Nicolas Lemery yritti selittää eri aineiden ominaisuuksia atomien muotojen avulla: esimerkiksi happojen hapan maku ja kyky syövyttää metalleja johtuivat hänen mukaansa siitä, että niiden atomit olivat piikikkäitä. Myös Isaac Newton oletti kaiken aineen koostuvan atomeista.[4] Boylen ansiosta atomimalli sai uutta huomiota osakseen, sillä Demokritoksen atomimalli oli likimain unohtunut.
Sveitsiläinen fyysikko Daniel Bernoulli julkaisi vuonna 1738 teoksen nimeltä Hydrodynamica, joka oli pohja kineettisen kaasuteorian synnylle. Bernoullin mukaan kaasut koostuvat pienistä hiukkasista, jotka ovat koko ajan liikkeessä sekä törmäilevät jatkuvasti toisiinsa. Bernoullin mukaan kaasujen paine johtuu nimenomaan rakenneosasten keskinäisistä törmäyksistä sekä näiden törmäyksistä astian seinämiin, ja kaasun lämpötila riippuu vastaavasti näiden liikkuvien hiukkasten nopeudesta. Teoria tuli kuitenkin yleisesti hyväksytyksi vasta seuraavalla vuosisadalla.[6]
Kemiaan atomiteoriaa sovelsi menestyksellisesti John Dalton 1800-luvun alussa. Sen avulla hän selitti etenkin kerrannaisten painosuhteiden lain. Tämä laki sanoo, että jos kaksi alkuainetta muodostaa useampia yhdisteitä keskenään, niin ne määrät yhtä alkuainetta, jotka voivat yhtyä samaan määrään toista alkuainetta, ovat yksinkertaisessa, yleensä pienillä kokonaisluvuilla ilmaistavassa suhteessa toisiinsa.[7] Esimerkiksi 12 grammaa hiiltä voi yhtyä joko 16 grammaan happea muodostaen hiilimonoksidia tai tarkalleen kaksinkertaiseen määrään, 32 grammaan happea muodostaen hiilidioksidia. Tämä selittyy sillä, että hiilimonoksidin molekyylissä on yksi hiili- ja yksi happiatomi, hiilidioksidin molekyylissä taas yksi hiili- ja kaksi happiatomia.
Tämän teorian ja kemiallisten reaktioiden avulla pystyttiin jo 1800-luvun alkupuolella määrittämään varsin tarkoin eri alkuaineiden atomien massojen suhteet toisiinsa.[8] Ei kuitenkaan vielä tiedetty, kuinka suuria niiden massat olivat gramman murto-osina, vain niiden suhteelliset massat tunnettiin. Siksi olikin otettava käyttöön erityinen atomimassayksikkö, joka alkujaan määriteltiin vetyatomin massaksi. (Nykyisin se on määritelty 1/12-osaksi hiili-12-atomin massasta.) Samoihin aikoihin kehittyivät nopeasti myös lämpöoppi ja siihen läheisesti liittyvä kineettinen kaasuteoria, joka myös edellytti kaasun koostuvat molekyyleistä.[9] Kineettiseen kaasuteoriaan perustuva Avogadron laki osoittautui myös hyödylliseksi kaasumaisten alkuaineiden atomimassojen määrityksessä.
1800-luvulla atomiteoria sai kuitenkin erityisen suuren merkityksen orgaanisessa kemiassa. Erilaisten kemiallisten reaktioiden avulla tehtiin pitkälle meneviä päätelmiä orgaanisten molekyylien rakenteesta ja siitä, missä järjestyksessä niissä atomit sijaitsevat toisiinsa nähden. Kun paljon myöhemmin orgaanisten molekyylien rakenteita pystyttiin tutkimaan myös röntgensäteiden avulla, kemistien tekemät päätelmät osoittautuivat useimmissa tapauksissa oikeiksi. [10]
Atomiteoria tuli varsinkin orgaanisen kemian tutkijoiden yleisesti hyväksymäksi, mutta useat fyysikot, esimerkiksi Ernst Mach ja Wilhelm Ostwald, pitivät sitä vielä 1800-luvun lopullakin tarpeettomana hypoteesina. Vasta radioaktiivisuutta koskevat tutkimustulokset sekä Albert Einsteinin vuonna 1905 esittämä Brownin liikkeen selitys ratkaisivat kiistan lopullisesti ja tekivät myös mahdollisiksi määrittää atomimassayksikön ja gramman välisen suhteen.[11]
Demokritoksen tavoin myös Dalton ja tiedeyhteisö vielä kauan hänen jälkeensäkin piti atomia jakamattomana. Elektrolyysin tutkimus johti kuitenkin vähitellen siihen päätelmään, että atomi voi saada sähkövarauksen eli ionisoitua,[12] mikä antoi aihetta olettaa, että on olemassa atomiakin pienempiä sähköisesti varattuja hiukkasia.
1900-luvun atomimallit[muokkaa | muokkaa wikitekstiä]


Tutkittuaan sähkön kulkua katodisädeputken tyhjiössä Sir Joseph Thomson keksi elektronin vuonna 1897. Thomson oletti, että elektronit ovat osa atomia, niinpä hän julkaisi vuonna 1904 ensimmäisen elektronit sisältävän atomimallin. Siinä atomi esitettiin kimmoisana, positiivisena pallona, jonka sisällä on negatiivisia elektroneita. Ulospäin atomi oli sähköisesti neutraali.[13] Koska atomin oli havaittu lähettävän sähkömagneettista säteilyä ja lisäksi tiedettiin sähköisen varauksen kiihtyvän liikkeen aiheuttavan säteilyä, Thomson päätteli elektronien värähtelevän atomin sisällä ja näin myös säteilevän.
Vuonna 1909 uusiseelantilainen ydinfysiikan pioneeri Ernest Rutherford päätti testata Thomsonin atomimallin erityisellä sirontakokeella. Hän pommitti ohutta kultalevyä alfa-hiukkasilla ja seurasi niiden siroamista kultalevyyn törmäämisen jälkeen. Koska suurin osa positiivisesti varautuneista alfahiukkasista ei muuttanut kulkusuuntaansa mutta osa niistä muutti suuntaansa jopa yli 90 astetta, Rutherford esitti, että atomissa on pieni positiivinen ydin ja sitä ympäröivä negatiivinen elektroniverho.[14] Rutherfordin atomimallia voi verrata aurinkokuntaan, jossa aurinko vastaa atomin ydintä ja planeetat elektroneita. Rutherford myös väitti, että ydintä kiertävien elektronien keskeiskiihtyvyys aiheutti kokeissa havaitun atomin säteilyn.
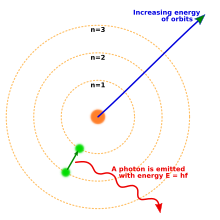
Ernest Rutherfordin oppilaana englannissa opiskellut tanskalaisfyysikko Niels Bohr korjaili ja tarkensi Rutherfordin atomimallia. Hän sai aikaan mallin, jota vieläkin käytetään esimerkiksi kouluissa selkeytensä ja yksinkertaisuutensa vuoksi, vaikkei se vastaakaan todellisuutta täydellisesti. Merkittävin muutos on Bohrin tuoma käsitys, että elektroneilla on vain tiettyjä määrättyjä kiertoratoja atomissa, ja jokainen rata edustaa tiettyä energiatilaa. Näin ollen elektroni, joka siirtyy ulommalta radalta ydintä lähempänä olevalle radalle, luovuttaa energiaansa sähkömagneettisena säteilynä.[15] Tämä kumosi täysin Rutherfordin teorian keskeiskiihtyvyyden säteilyvaikutuksesta. Jokaista elektronin mahdollista siirtymistä radalta toiselle vastaa yksi spektriviiva atomin spektrissä.
Bohrin malli on kuitenkin puutteellinen; se ei päde kuin vetyatomille ja yksielektroniselle atomille. Näissäkään tapauksessa se ei selitä atomien spektrien hienorakennetta. On nimittäin osoittautunut, että esimerkiksi Balmerin sarjan mukaiset spektriviivat muodostuvat itse asiassa useammasta lähellä toisiaan olevasta, mutta toisistaan erottuvasta viivasta. Tämän selittämiseksi Arnold Sommerfeld esitti vuonna 1915 tarkennetun atomimallin, jonka mukaan elektronien kiertoradat eivät välttämättä ole ympyröitä vaan ne voivat olla myös ellipsejä. Bohrin teorian mukaisen pääkvanttiluvun lisäksi oli otettava käyttöön myös sivukvanttiluku, jonka Sommerfeldin mallissa tulkittiin kuvaavan radan eksentrisyyttä. Lisäksi suhteellisuusteorian tuloksista seurasi, että ellipsit jatkuvasti kiertyivät tasossaan eli niissä esiintyi periheliliike.[16]
Erwin Schrödinger korvasi myöhemmin Bohrin ja Sommerfeldin mallit kvanttimekaanisella atomimallilla, jonka mukaan elektroneilla ei ole määritettävissä olevia kiertoratoja, vaan niillä on tietty todennäköisyys sijaita tietyssä avaruuden pisteessä.
Katso myös[muokkaa | muokkaa wikitekstiä]
Lähteet[muokkaa | muokkaa wikitekstiä]
- ↑ a b c John Hudson: Suurin tiede – kemian historia, s. 23–24. Suomentanut Kimmo Pietiläinen. Art House, 2002. ISBN 951-884-346-5.
- ↑ Hudson, s. 29
- ↑ Hudson, s. 32
- ↑ a b Michael H. Hart: Ihmiskunnan 100 suurinta, Maailmanhistorian sata merkittävintä henkilöä tärkeysjärjestyksessä, s. 408–411. Art House, 1979. ISBN 951-99229-1-1.
- ↑ Hudson, s. 74.
- ↑ Baeyer, Hans Christian von: Maxwellin demoni, s. 79–82. Suomentanut Hannu Karttunen. Art House, 2000. ISBN 951-884-321-X.
- ↑ Hudson, s. 130.
- ↑ Hudson, s. 128–140.
- ↑ Baeyer, s. 82–84.
- ↑ Feynman, Richard P.: Suhteellisen helppoa: Seitsemän lukua fysiikkaa. Suomentanut Kimmo Pietiläinen. Ursan julkaisuja n:o 82. 2002. ISBN 952-5329-18-6
- ↑ Hudson, s. 311–312.
- ↑ Hudson, s. 325–326.
- ↑ Hudson, s. 245
- ↑ Hudson, s. 258
- ↑ Hudson, s. 264
- ↑ K. V. Laurikainen, Uuno Nurmi, Rolf Qvickström, Erkki Rosenberg, Matti Tiilikainen: Lukion fysiikka 2, s. 83, 158. WSOY, 1973. ISBN 951-0-05657-X.